
 ijѧУ����С����Խ̲���ͭ��Ũ���ᷴӦ������ˡ��ܹ���ͭ��Ӧ����������Ũ���Ƕ��٣�����̽�����⣬����������·�������ʵ�飺ʵ���Լ���18mol/L����20mL����ͭ������������2mol/LNaOH��Һ��
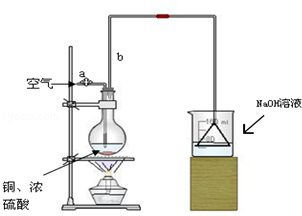
ijѧУ����С����Խ̲���ͭ��Ũ���ᷴӦ������ˡ��ܹ���ͭ��Ӧ����������Ũ���Ƕ��٣�����̽�����⣬����������·�������ʵ�飺ʵ���Լ���18mol/L����20mL����ͭ������������2mol/LNaOH��Һ������ ��1��������װ�õ�ʵ����Ҫ�ڿ�ʼʱ���װ�õ������ԣ�
��2��SO2����Ⱦ�����岻���ŷŵ������У���������������ܺͼ�Һ��Ӧ�����Σ�
β���������л������õ�װ���ܷ�������
��3����ƿ����Cu��Ũ������ȷ�Ӧ����CuSO4��SO2��H2O��װ���г������ܼ��������������ã�ʹˮ��������������
��4������H2O2��Na2SO3����ΪNa2SO4������BaCl2��Һ��Ӧ����BaSO4������ͨ�����ˡ�ϴ�ӡ�����õ�������������SԪ�����ʵ���������SԪ���غ��ϻ�ѧ����ʽ������Ҫ��Ӧ���������Ũ�ȣ�
��5��������H2O2������ΪBaSO3��BaSO4���������ܼ�����Ԫ�����ʵ�������ʵ�������
��� �⣺��1����װ��������װ�ã�ʵ��ǰӦ�ü���װ�������ԣ���������������ݳ���ò����������ʴ�Ϊ������װ�������ԣ�
��2��SO2����Ⱦ�����岻���ŷŵ������У���������������ܺͼ�Һ��Ӧ�����Σ�����NaOH������������δ��Ӧ��SO2��
β���������л������õ�װ���ܷ����������µ�©���Ϳڴ��л������ã��ܷ�������
�ʴ�Ϊ��SO2����������
��3����ƿ����Cu��Ũ������ȷ�Ӧ����CuSO4��SO2��H2O����Ӧ����ʽΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��װ���г������ܼ��������������ã�ʹˮ��������������
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O�������ܣ�
��4��������������������������Ϊ�����ƣ������Ȼ�����Һ��Ӧ�������ᱵ������ͨ�����ˡ�ϴ�ӡ�����õ��������������������Ϊ13.98gΪ���ᱵ���������ʵ���=$\frac{13.98g}{233g/mol}$=0.06mol��������Ԫ���غ㣬������������Ϊ0.06mol�����ݻ�ѧ����ʽ��֪��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O����Ӧ���������ʵ���Ϊ0.12mol��ʣ���������ʵ���=18mol/L��0.020L-0.12mol=0.24mol��ʣ����Ҫ�����Ũ��=$\frac{0.24mol}{0.02L}$=12mol/L��
�ʴ�Ϊ�����ˣ�ϴ�ӣ����12mol/L��
��5��������������⣬����Ϊ�����ᱵ�����ᱵ���������ܼ�����Ԫ�����ʵ�����������Ҫ����������⣬������������Ϊ�����ƺ��ٽ��г����������㣬
�ʴ�Ϊ����Ҫ�����ձ������ɵ�Na2SO3���ܱ���������ΪNa2SO4�����������˫��ˮ��ֱ�Ӳⶨ������������ȷ��SԪ�ص����ʵ������Ӷ�ʹʵ��������
���� ������Ũ�����Cu�ķ�ӦΪ���忼������ʵ�鷽����ƣ�Ϊ��Ƶ���㣬��ȷʵ��ԭ����ʵ���������ԭ�������������ǽⱾ��ؼ���ע���ʵ���еij����ܵ����ã�Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CH4 | B�� | CO2 | C�� | NaHCO3 | D�� | CH3COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ�����ģ�ʡ�Լг�װ�ã� | ��Ӧʵ�� |
| A | �ձ�����������ʯ�������ƾ��� | Ũ���ᾧ����ͭ��Һ�Ƶ��� |
| B | �ձ�������������ͷ�ιܡ�©������ֽ | �������ȥ���ᱵ�е�����̼�ᱵ |
| C | �ձ�������������ͷ�ιܡ�����ƿ | �ù����Ȼ�������100 mL 0.5 mol•L-1����Һ |
| D | �ձ�������������ͷ�ιܡ���Һ©�� | ����ˮ��CCl4��ȥNaBr��Һ�е�����NaI |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
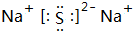 ��W2X2�ĽṹʽH-O-O-H��
��W2X2�ĽṹʽH-O-O-H���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���н϶�H+����Һ | B�� | pH��7����Һ | ||
| C�� | c��OH-����c��H+������Һ | D�� | �μӷ�̪����ɫ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ζ����������˿�� | |
| B�� | ����ɫ��Ӧ����NaCl��Na2SO4 | |
| C�� | �ö����ЧӦ����Fe��OH��3�����FeCl3��Һ | |
| D�� | �ü��ȵķ�������Na2CO3��NaHCO3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 12% | B�� | 32% | C�� | 44% | D�� | 88% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | c��NO��/mol•L-1 | c��H2��/mol•L-1 | ����/mol•L-1•min-1 |
| �� | 0.0060 | 0.0010 | 1.8��10-4 |
| �� | 0.0060 | 0.0020 | 3.6��10-4 |
| �� | 0.0010 | 0.0060 | 3.0��10-5 |
| �� | 0.0020 | 0.0060 | 1.2��10-4 |
| A�� | ������Ӧ�ٶ��ɵڢٲ���Ӧ���� | |
| B�� | ����Ӧ�Ļ��һ���Ǣ٣��� | |
| C�� | �÷�Ӧ���ʱ���ʽ��v=5000c2��NO��•c��H2�� | |
| D�� | �÷�Ӧ���Ȼ�ѧ����ʽΪ2NO��g��+2H2��g���TN2��g��+2H2O��g����H=-664kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | ֻ�Т� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com