
【题目】NaNO2是一种食品添加剂,具有致癌性。酸性KMnO4溶液与NaNO2反应的化学方程式为:MnO4+NO2+□→ Mn2++NO3+H2O(未配平)。下列叙述中正确的是
A. 该反应中NO2被还原 B. 生成1 mol NaNO3需消耗0.4 mol KMnO4
C. 反应过程中溶液的酸性增强 D. □中的粒子是OH
【答案】B
【解析】
该反应中Mn元素化合价由+7价变为+2价,所以MnO4-是氧化剂,NO2-应该作还原剂,亚硝酸根离子中N元素应该失电子化合价升高,生成硝酸根离子,根据转移电子相等、原子守恒配平方程式为2MnO4-+5NO2-+6H+=2Mn2++5 NO3-+3H2O。A.该反应中N元素化合价由+3价变为+5价,所以亚硝酸根离子失电子被氧化,故A错误;B.根据转移电子守恒得,生成1molNaNO3需消耗KMnO4的物质的量= ![]() =0.4mol,故B正确;C.根据元素守恒、电荷守恒知,
=0.4mol,故B正确;C.根据元素守恒、电荷守恒知,![]() 中是H+,氢离子参加反应导致溶液中氢离子浓度降低,则溶液的酸性减弱,故C错误;D.由C分析可知,
中是H+,氢离子参加反应导致溶液中氢离子浓度降低,则溶液的酸性减弱,故C错误;D.由C分析可知,![]() 中是H+,故D错误;故选B。
中是H+,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 铅蓄电池放电时的负极和正极的质量均增加
B. MgO(s)+C(s)![]() Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
Mg(s)+CO(g)在室温下不能自发进行,说明该反应的△H <0
C. 对于发应2H2O2![]() 2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率
D. H2O与金属Na反应生成1molH2,反应中转移的电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.lmol/L的K2CO3溶液中,由于CO32-的水解,使得c(CO32-)<0.lmol/L。如果要使c(CO32-)更接近于0.lmol/L,可以采取的措施是( )
A.加入少量盐酸 B.加入适量的水 C.加入适量的KOH D.加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近浙江大学成功研制出具有较高能量密度的新型铝一石墨烯(Cn)电池(如图)。该电池分别以铝、石墨烯为电极,放电时电池中导电离子的种类不变。已知能量密度=电池容量(J)÷负极质量(g)。下列分析正确的是
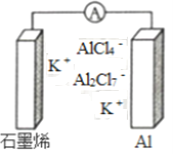
A. 放电时,Cn(石墨烯)为负极
B. 放电时,Al2Cl7-在负极转化为AlCl4-
C. 充电时,阳极反应为4 Al2Cl7-+3e-=A1+7AlCl4-
D. 以轻金属为负极有利于提高电池的能量密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用下列装置探究Na与CO2反应的还原产物,已知PdCl2+CO+H2O==Pd(黑色)↓+CO2+2HCl。下列相关分析错误的是
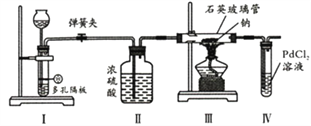
A. I中发生反应可以是Na2CO3+H2SO4==Na2SO4+H2O+CO2↑
B. II中浓硫酸的目的是干燥CO2
C. 实验时,III中石英玻璃管容易受到腐蚀
D. 步骤IV的目的是证明还原产物是否有CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.ⅠA族元素单质的熔点从上往下逐渐降低
B.分子晶体中一定存在共价键
C.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
D.同周期非金属氧化物对应的水化物的酸性从左往右依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2可用于电子、仪表等工业。以毒重石(主要成分BaCO3,含少量CaCO3、MgSO4、Fe2O3、SiO2等杂质)为原料,模拟工业提取BaCl2·2H2O的流程如下:
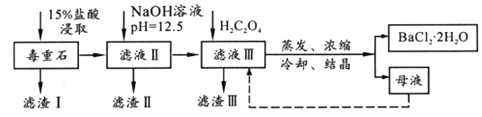
已知:(1)Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(2)离子浓度小于至1×10-5认为沉淀完全。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.0 | 3.7 |
(1)滤渣I的成分为________(填化学式),过滤所需玻璃仪器有______________。
(2)加入NaOH溶液后所得滤液III中,含有的Mg2+浓度为_____;加入H2C2O4时应避免过量,其原因是__________________________________。
(3)BaCl2母液中除了含有Ba+、Cl-外,还含有大量的______(填离子符号)。有人从“绿色化学”角度设想将“母液”沿虚线进行循环使用,请分析在实际工业生产中是否可行,_______(填“可行”或“不可行”),理由是_______________________。
(4)滤渣III是结石的主要成分,现将滤渣III 经过洗涤干燥后在有氧环境下进行热重分析,取146.0g灼烧,所得参数如下表。
溫度(℃) | 常温 | 190200 | 470480 |
质量(g) | 146.0 | 128.0 | 100.0 |
滤渣III 的成分是__________(填化学式);200~470℃时发生反应的化学方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,![]() 是一种淡黄色的油状液体
是一种淡黄色的油状液体![]() 下列对
下列对![]() 的有关叙述正确的是
的有关叙述正确的是![]()
A. ![]() 分子是由极性键构成的非极性分子
分子是由极性键构成的非极性分子
B. ![]() 分子的空间构型为平面三角形
分子的空间构型为平面三角形
C. NF3分子的稳定性较NCl3强
D. ![]() 的沸点比
的沸点比![]() 的沸点低是因为
的沸点低是因为![]() 比
比![]() 键键能小
键键能小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以溴乙烷为原料,用下述六种反应的类型:(1)氧化(2)消去(3)加成(4)酯化(5)水解(6)加聚来合成乙二酸乙二酯的正确顺序
A. (1)(5)(2)(3)(4) B. (1)(2)(3)(4)(5)
C. (2)(3)(5)(1)(4) D. (2)(3)(5)(1)(6)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com