
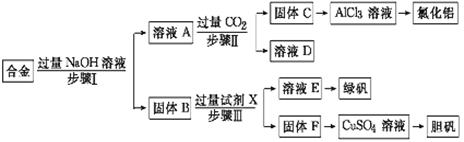
为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
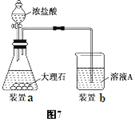
(3)进行步骤Ⅱ时,该小组用如图7所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
【知识点】物质的分离和提纯 金属及其化合物的性质J2 C5
【答案解析】(1)2Al+2OH—+2H2O=2AlO2-+3H2↑(2分)
(2)稀硫酸或H2SO4(2分) 过滤(2分)
(3)在装置Ⅰ、Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶(合理答案即给分)(2分)
(4)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O(2分)
途径②最佳,理由是原料利用率高,环境污染小(2分,结论1分,理由1分)
解析:(1)步骤Ⅰ加过量的氢氧化钠,金属铝和氢氧化钠反应,即2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)步骤Ⅰ、Ⅱ、Ⅲ均是固体和液体的分离操作,应该是过滤;
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个除去氯化氢的装置,所以可在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢;
(4)铜和硝酸反应生成硝酸铜、一氧化氮和水,即3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所以途径②最佳。
【思路点拨】本题考查了物质的分离和提纯,掌握铝、铁和铜及其化合物的性质是解答本题的关键。


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
利用反应Cu+2FeCl3===CuCl2+2FeCl2组成一个化学电池。
(1)指出正极为________,电极反应式为__________________________________;负极为____________,电极反应式为____________________________。
(2)若电池内溶液为100 mL 0.5 mol/L的FeCl3溶液;当溶液中FeCl3全部被还原成FeCl2时,溶液中CuCl2的物质的量浓度是________,导线上通过的电子是________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度低于570℃时反应的化学方程式 。
(2)中学教材中用右图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是
。
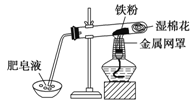
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图发生该反应并有氢气的收集装置图(包括反应时容器中的物质)。
 |
说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽:
 试管:
试管:
 蒸发皿:
蒸发皿:
 玻璃导管:
玻璃导管:
 或
或
 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)乙同学为了探究实验后的固体产物是否存在Fe3O4(假定铁全部反应完全)设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液X中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2符合 关系时,才能确定固体样品中一定只存在Fe3O4。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据陈述的知识,类推得出的结论正确的是
A.镁条在空气中燃烧生成的氧化物是MgO,则钠在空气中燃烧生成的氧化物是Na2O
B. Fe与S直接化合生成FeS,则Cu与S直接化合生成Cu2S
C.少量CO2通入Ca(ClO)2溶液生成CaCO3,则少量SO2通入Ca(ClO)2溶液生成CaSO3
D. 已知第四主族沸点CH4<SiH4<GeH4,则第六主族沸点H2O<H2S<H2Se
查看答案和解析>>
科目:高中化学 来源: 题型:
、将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g.则下列叙述中不正确的是( )
A.当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100mL
B.当金属全部溶解时收集到NO气体的体积一定为2.24L
C.参加反应的金属的总质量为9.6g>m>3.6g
D.当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
230Th和232Th是钍的两种同位素,232Th可以转化成233U。下列有关Th的说法正确的是 ( )
A.Th元素的质量数是232
B.Th元素的相对原子质量是231
C.232Th转化成233U是化学变化
D.230Th和232Th的化学性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常用电解熔融氯化钠的方法制取金属钠和氯气,试回答下列问题:
(1) 金属钠在 阴 极上产生。
(2) 写出产生Cl2的电极反应方程式:
2Cl--2e- Cl2↑ 。
Cl2↑ 。
(3) 该反应 是 (填“是”或“不是”)离子反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
M5纤维是近年来开发出的一种超高性能纤维,它比现有的防爆破材料轻35%,用它制成的头盔、防弹背心和刚性前后防护板,能为武装人员提供更多的生命保障。下面是M5纤维的合成路线(部分反应未注明条件):
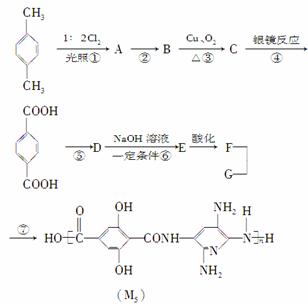
已知:当反应条件为光照且与X2反应时,通常是X2与烷烃基或苯环侧链烃基上的氢原子发生取代反应,而当反应条件为催化剂存在且与X2反应时,通常为苯环上的氢原子直接被取代。
根据上述合成M5纤维的过程,完成下列问题:
(1)合成M5纤维的单体G的结构简式为
________________________________________________________________________
________________________________________________________________________,
F的含氧官能团的名称有
________________________________________________________________________。
(2)在①~⑦的反应中,不属于取代反应的是______________,②的反应条件是
________________________________________________________________________。
(3)生成A的同时可能生成的A的同分异构体为
________________________________________________________________________。
(4)1 mol的C和足量新制的氢氧化铜悬浊液反应可以生成________ mol砖红色沉淀。
(5)1 mol F和Na2CO3溶液反应最多消耗Na2CO3______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基钠和氢化钠与水反应的化学方程式如下:
①NaNH2+H2O=NaOH+NH3↑ ② NaH+H2O=NaOH+H2↑。下列叙述正确的是
A.方程式②中,每生成1mol H2转移2 mol电子
B.①和②两个反应都是氧化还原反应
C.氨基钠和氢化钠与盐酸反应都只生成一种盐
D.氨基钠和氢化钠晶体中都有离子键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com