
 某溶液中可能大量含有Mg2+,Cu2+,Al3+,Cl-,OH-,CO32-.当加入氢氧化钠溶液时,生成白色沉淀的物质的量与加入氢氧化钠的物质的量关系如图所示.
某溶液中可能大量含有Mg2+,Cu2+,Al3+,Cl-,OH-,CO32-.当加入氢氧化钠溶液时,生成白色沉淀的物质的量与加入氢氧化钠的物质的量关系如图所示.

科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、1 mol S(g)与O2(g)完全反应生成SO2(g),反应放出的热量小于297.0 kJ | ||
B、一定条件下1 mol SO2(g)和
| ||
| C、在相同条件下,SO2 (g)比SO3 (g)稳定 | ||
D、S(s)与O2(g)反应生成SO3(g)的热化学方程式S(s)+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
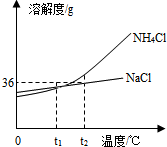 如图是氯化铵和氯化钠两种固体物质的溶解度曲线,下列叙述错误的是( )
如图是氯化铵和氯化钠两种固体物质的溶解度曲线,下列叙述错误的是( )| A、t2℃时,向18g NaCl固体加入50g水,充分搅拌后固体能全部溶解 |
| B、0℃时,NaCl和NH4C1两种物质的饱和溶液都升温至t1℃,两种溶液中溶质的质量分数相等 |
| C、t2℃时,将NH4Cl溶液降温到0℃,不一定有晶体析出 |
| D、NH4Cl中含有少量NaCl,可以用冷却热饱和溶液的方法提纯NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:
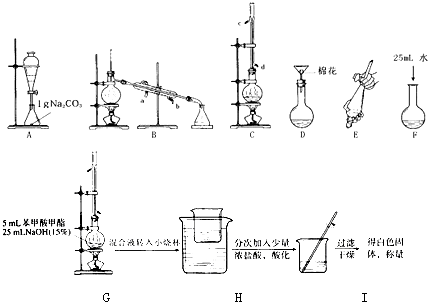
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g?cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度下,反应2NaCl(s)═2Na(s)+Cl2(g)的△H<0,△S>0 |
| B、NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C、常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| D、由于Ksp(BaSO4)<Ksp(BaCO3),因此不可能使BaSO4沉淀转化为BaCO3沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Fe3+、K+、NO3- |
| B、NH4+、Al3+、NO3-、Cl- |
| C、K+、AlO2-、Na+、SO42- |
| D、K+、NO3-、Na+、Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com