


科目:高中化学 来源: 题型:
| A、氯化钾 | B、氯化汞 |
| C、氯化镁 | D、氯化钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热后观察是否有气体产生 |
| B、溶于水后滴加稀氯化钙溶液观察是否有沉淀产生 |
| C、溶于水后检验溶液是否显碱性 |
| D、溶于水后通入CO2观察是否有NaHCO3产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
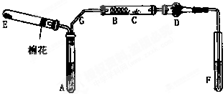 如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 将少量Fe(NO3)2试样加水溶解,滴加稀H2SO4酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2试样已变质 |
| B | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
| C | 分别测定常温下0.1mol?L-1Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 向浓度均为0.1mol?L-1NaCl和NaI混合溶液中,滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于1:1 |
| B、小于1:1 |
| C、大于1:1 |
| D、小于或等于1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气可用于漂白,是因为氯气有强氧化性 |
| B、工业用石灰石、纯碱和石英在高温下制得玻璃的原理与硅酸和碳酸的酸性强弱有关 |
| C、神七宇航员所穿航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材 |
| D、硫酸工业中,从吸收塔上部导出的气体再次通入接触室进行二次氧化,进一步吸收后,二氧化硫的含量很少,可直接排放到空气中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com