
| A. | 标准状况下,22.4 L H2O含有的分子数为 NA | |
| B. | 28g N2和N4组成的混合气体中含有的原子数为2 NA | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3 NA | |
| D. | 2.3 g Na与足量水反应,转移的电子数目为0.2 NA |
分析 A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B.28g混合气体中含有28g氮原子,含有2mol氮原子;
C.氯化铝溶液的体积不知,无法计算溶液中氯离子的物质的量;
D.2.3g钠的物质的量为0.1mol,钠为1价计算,0.1mol钠完全反应失去0.1mol电子.
解答 解:A.标况下,水不是气体,题中条件无法计算22.4L水的物质的量,故A错误;
B.28gN2和N4组成的混合气体中中含有28gN原子,含有的氮原子的物质的量为2mol,含有的原子数为2NA,故B正确;
C.没有告诉1mol•L-1 AlCl3溶液的体积,无法计算溶液中氯离子的数目,故C错误;
D.钠为1价金属,2.3g钠的物质的量为0.1mol,完全反应失去了0.1mol电子,转移的电子数目为0.1NA,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的判断及计算,题目难度中等,注意明确标准状况下气体摩尔体积的使用条件,掌握物质的量与阿伏伽德罗常数、摩尔质量之间的转化关系.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:解答题
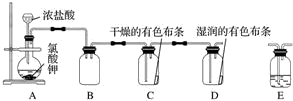
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有还原性,可用于蔗糖脱色 | |
| B. | 双氧水具有强氧化性,可用于杀菌消毒 | |
| C. | 铁粉表面积大,可用作食品干燥剂 | |
| D. | SiO2具有导电性,可用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火时使用泡沫灭火器灭火 | |
| B. | 明矾常用于水体的净化、杀菌和消毒 | |
| C. | 热的纯碱溶液去污效果更好 | |
| D. | 84消毒液与洁厕灵混合后用于清洁洗手间的效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
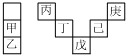 甲~庚等主族元素在周期表中的相对位置如下表,己的最高价氧化物对应的水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等主族元素在周期表中的相对位置如下表,己的最高价氧化物对应的水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 气态氢化物的稳定性:庚<己<戊 | |
| B. | 庚与戊的原子序数相差24 | |
| C. | 庚与甲形成的单核离子半径大小为:庚<甲 | |
| D. | 丁的最高价氧化物可用于制造计算机的芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 82克O2所含有的原子数目为NA | |
| B. | 0.5molH2O含有的原子数目为1.5NA | |
| C. | 1molH2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{K}_{w}}{c(O{H}^{-})}$=0.1mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| B. | 遇苯酚显紫色的溶液:I-、K+、SCN-、Mg2+ | |
| C. | 与铝反应产生大量氢气的溶液:NH4+、Na+、CO32-、NO3- | |
| D. | 加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前使用的元素周期表中,最长的周期含有36种元素 | |
| B. | 只有在原子中,质子数才与核外电子数相等 | |
| C. | 金属元素与非金属元素能形成共价化合物 | |
| D. | 非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com