
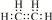 .
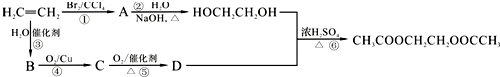
.分析 根据题中各物质转化关系,乙烯与溴发生加成生成A为CH2Br-CH2Br,A发生碱性水解生成乙二醇,乙烯与水发生加成生成B为CH3CH2OH,B氧化得C为CH3CHO,C氧化得D为CH3COOH,D与乙二醇发生酯化生成,据此答题.
解答 解:根据题中各物质转化关系,乙烯与溴发生加成生成A为CH2Br-CH2Br,A发生碱性水解生成乙二醇,乙烯与水发生加成生成B为CH3CH2OH,B氧化得C为CH3CHO,C氧化得D为CH3COOH,D与乙二醇发生酯化生成,
(1)乙烯的电子式 为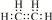 ,
,
故答案为: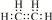 ;
;
(2)B为CH3CH2OH,B分子中的官能团名称是羟基,
故答案为:羟基;
(3)根据上面的分析可知,反应②为取代反应,反应③加成反应,
故答案为:取代反应;加成反应;
(4)反应①的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br,反应⑥的化学方程式为2CH3COOH+HOCH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2OOCCH3+2H2O,
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;2CH3COOH+HOCH2CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH2OOCCH3+2H2O.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸性质与转化,注意对基础知识的理解掌握,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、Fe3+、Br-、NO3-可以大量共存 | |
| B. | 和足量的Ba(OH)2溶液反应的离子方程式:2NH4++Fe2++2SO42-+2Ba2++4OH-═2NH3•H2O+Fe(OH)2↓+2BaSO4↓ | |
| C. | 和KMnO4溶液反应后溶液可以褪为无色 | |
| D. | 该溶液与氢氧化钠溶液共热,产生的气体能使湿润的蓝色石蕊试纸变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质及变化 | 描述 | 相关知识 | |
| A | 碘化钾溶液滴到土豆片上 | 变蓝色 | 土豆片含淀粉 |
| B | 煤的气化 | 化学变化 | 主要反应是碳与水生成水煤气等 |
| C | 乙烯和苯 | 都能使溴水褪色 | 分子中含有相同的碳碳双键 |
| D | 蔗糖和麦芽糖 | 多糖 | 二者互为同分异构体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的密度随核电荷数的增加逐渐减小 | |
| B. | 单质的颜色随核电荷数的增加而逐渐变浅 | |
| C. | 单质的氧化性随核电荷数的增加而逐渐减弱 | |
| D. | 氢化物的稳定性随核电荷数的增加逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有卤代烃都是无色、难溶于水,比水重的液体 | |
| B. | 所有卤代烃在适当条件下都能发生取代反应 | |
| C. | 所有卤代烃在适当条件下都能发生消去反应 | |
| D. | 氟氯代烷(即氟利昂)是优良的制冷剂、灭火剂,需推广使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
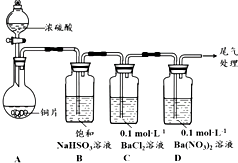
| 序号 | 实验操作 | 实验现象 |
| 1 | 取0.3g 纯净Na2SO3固体,向其中加入10mL2mol•L-1盐酸,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,4min后,溶液变浑浊 |
| 2 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,2h后,溶液变浑浊 |
| 3 | 取0.3g 纯净Na2SO3固体,向其中加入10mL 浓HNO3,再滴入4滴BaCl2溶液 | 产生红棕色气体;滴入BaCl2溶液后,溶液立即产生大量白色沉淀 |
| 序号 | 实验操作 | 实验现象 |
| 4 | 取固体混合物,向其中加入10mL2mol•L-1 HNO3,再滴入4滴BaCl2溶液 | 产生无色气泡;滴入BaCl2溶液后,开始无现象,20min后,溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备1mol HRO3转移电子数一定为2NA | |
| B. | R、Z简单离子的还原性:Z(离子)<R(离子) | |
| C. | HZ分子的稳定性大于HR分子 | |
| D. | HRO3与HZ计量数之比为1:5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com