
完成下列计算
(1) 相同物质的量的O2和O3的质量比____,分子个数比为______,所含氧原子的个数比为_______.
(2) 在200 mL 2 mol/L MgCl2溶液中,溶质的质量为________.此溶液中Mg2+的物质的量浓度为___________,Cl-的物质的量浓度为________.
(3) 在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________.
(1)2:3, 1:1 ,2:3(2)38g ,2mol/L 4mol/L(3)1:8
【解析】
试题分析:(1)根据m=nM可知,相同物质的量的O2和O3的质量之比=32g/mol:48g/mol=2:3,由N=nN可知,分子数目之比等于物质的量之比=1:1;氧气所含氧原子数目为氧气分子2倍,臭氧所含氧原子数目为臭氧分子的3倍,故相同物质的量的O2和O3含有氧原子数目之比=1×2:1×3=2:3,故答案为:2:3;1:1;2:3;(2)200mL 2mol?L-1MgCl2溶液中,氯化镁的物质的量为:2mol?L-1×0.2L=0.4mol,氯化镁的质为:95g/mol×0.4mol=38g,此溶液中Mg2+的物质的量浓度为:c(Mg2+)=c(MgCl2)=2mol?L-1, 此溶液中Cl-的物质的量浓度为:c(Cl-)=2c(MgCl2)=4mol?L-1,故答案为:38g;2mol?L-1;4mol?L-1.(3)假设溶液质量为100g,则KOH的质量=100g×28%=28g,故水的质量=100g-28g=72g,故KOH的物质的量=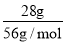 =0.5mol、水的物质的量=
=0.5mol、水的物质的量=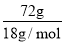 =4mol,故溶液中OH-与H2O数目之比=0.5mol:4mol=1:8
=4mol,故溶液中OH-与H2O数目之比=0.5mol:4mol=1:8
考点:物质的量的相关计算


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源:2014-2015学年湖南省高一上学期第一次阶段考试化学试卷(解析版) 题型:填空题
写出下列反应的离子方程式。
①稀硫酸与NaOH溶液反应的离子方程式:
________________________________________________________________________
②足量稀硝酸与CaCO3溶液反应的离子方程式:
________________________________________________________________________
③锌与稀硫酸反应的离子方程式:
________________________________________________________________________
④稀硫酸和氢氧化钡溶液反应的离子方程式:
⑤等体积等物质的量浓度的碳酸氢钠溶液和氢氧化钡溶液反应的离子方程式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁沈阳铁路实验中学高二上学期第一次月考化学试卷(解析版) 题型:选择题
25℃时的下列溶液中,碱性最强的是( )
A.pH=11的溶液 B.c(OH-)=0.12 mol/L的溶液
C.1 L含有4 g NaOH的溶液 D.c(H+)=1×10-10 mol/L的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁沈阳铁路实验中学高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列事实能说明醋酸是弱酸的是
① 醋酸钠溶液中CH3COO-与CH3COOH共存
② 0.1 mol/L的醋酸钠溶液的pH值约为9
③ 等体积、等浓度的硫酸和醋酸溶液与氢氧化钠反应,硫酸溶液消耗的氢氧化钠多
④ 0.1mol/L的醋酸的pH值约为4.8
⑤ pH值等于4、体积相等的醋酸和盐酸,与等浓度NaOH溶液充分反应时,醋酸液消耗碱液多
A.①②④⑤ B.②④ C.②③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁沈阳铁路实验中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列配制1.0mol/L的NaOH溶液的操作不会造成误差的是
A.称量后转移固体时不小心把少量固体洒到烧杯外
B.干净的容量瓶又用蒸馏水洗涤了一遍
C.转移过程中不小心把几滴溶液滴在外面
D.加水定容时,加水过多,倒出后并恢复到刻度线水平
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁沈阳铁路实验中学高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是
A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用左手压住分液漏斗上口部,右手握住活塞部分,把分液漏斗倒转过来振荡。
B.静置,分液漏斗中溶液分层,下层呈紫红色上层几乎无色。
C.打开分液漏斗的活塞使全部下层液体沿承接液体的烧杯内壁慢慢流出。
D.最后继续打开活塞另用容器承接并保存上层液体。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁大连市高二上期中考试化学试卷(解析版) 题型:填空题
(10分)现有25℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中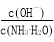 (增大、减小、不变)
(增大、减小、不变)
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
所得溶液的pH 7(填“>”“<”或“=”)。
(3)若向该氨水中加入氢氧化钠固体,则该电离平衡向 方向移动(分子化、离子化),电离平衡常数 。(增大、减小或不变)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁大连市高一上期中考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数, 下列说法正确的是
A、1.8g 水所含有的电子数目为NA
B、2g 氢气所含原子数为NA
C、常温常压下11.2L氧气所含分子数目为0.5NA
D、200 mL0.5mol·L-1 Na2SO4溶液所含Na+数目0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com