
| A. |  | B. | 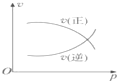 | C. |  | D. |  |
分析 A.温度高反应速率加快,正反应为放热反应,升高温度平衡逆向移动,C的体积分数减小;
B.交点前未到达平衡,压强增大平衡正向进行,交点处于平衡状态,再增大压强平衡向气体体积减小的方向移动,但瞬间正逆速率均增大;
C.催化剂不影响平衡移动;
D.正反应为放热反应,升高温度平衡逆向移动,A的转化率减小,正反应为气体体积减小反应,增大压强平衡正向移动,A的转化率增大.
解答 解:A.温度高反应速率加快,到达平衡时间缩短,正反应为放热反应,升高温度平衡逆向移动,C的体积分数减小,图象与实际相符合,故A正确;
B.交点前未到达平衡,压强增大平衡正向进行,交点处于平衡状态,再增大压强平衡向气体体积减小的方向移动,但瞬间正逆速率均增大,图象与实际不相符,故B错误;
C.使用催化剂加快反应速率,缩短到达平衡的水解,但使用催化剂不影响平衡移动,C的浓度不变,图象与实际不相符,故C错误;
D.正反应为放热反应,升高温度平衡逆向移动,A的转化率减小,正反应为气体体积减小反应,增大压强平衡正向移动,A的转化率增大,图象与实际不相符,故D错误,
故选:A.
点评 本题考查化学平衡影响因素与化学平衡图象问题,题目难度中等,关键是根据反应的特征判断外界条件对平衡移动的影响.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 酯类物质是形成水果香味的主要成分 | |
| B. | 用碳酸钠溶解鉴别乙醇、乙酸和乙酸乙酯 | |
| C. | 乙酸乙酯、油脂与NaOH溶液反应均有醇生成 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯净的甲烷在空气中燃烧可看到黄色火焰,用涂有澄清石灰水的小烧杯照在火焰上方,烧杯内壁变浑浊 | |
| B. | 检测孙老师是否酒后驾车,交警同志可用装有K2Cr2O7酸性试剂的吹气检测仪检测,看到检测仪由橙色变为绿色,说明孙老师酒后驾车应当进行处罚 | |
| C. | 科学探究:小米在家用食醋浸泡鸡蛋,观察到鸡蛋壳表面没有产生气泡,说明食醋主要成分乙酸没有酸性 | |
| D. | 天然纤维,人造纤维,合成纤维中均含有纤维素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C5H12属于烷烃且有三种同分异构体 | |
| B. | 乙酸、葡萄糖在一定条件下均能与Cu(OH)2反应 | |
| C. | 苯与浓硝酸、浓硫酸混合共热制取硝酸苯是发生取代反应 | |
| D. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaO | B. | ZnO | C. | Na2CO3 | D. | Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
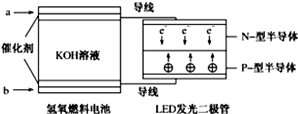 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )| A. | 氢氧燃料电池中OH-向b极移动 | |
| B. | 该装置中只涉及两种形式的能量转化 | |
| C. | H2在负极发生氧化反应 | |
| D. | P一型半导体连接电池负极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com