
【题目】下列说法正确的是
A. 需要加热才能发生的反应一定是吸热反应
B. 放热反应在常温下一定很容易发生
C. 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小
D. 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是
A.NH4+ 、Ag+、PO43-、Cl- B.Fe3+、H+、I-、HCO3-
C.K+、Na+、NO3- 、MnO4- D.Al3+、Mg2+ 、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀。最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如下,下列叙述错误的是
AgCl | AgI | Ag2S | |
Ksp | 1.8×10-10 | 8.51×10-16 | 6.3×10-50 |
A. 沉淀转化的实质就是沉淀溶解平衡的移动
B. 溶解度小的沉淀可以转化为溶解度更小的沉淀
C. AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶解程度相同
D. 25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 含金属元素的离子一定是阳离子
B. 金属阳离子被还原一定得到金属单质
C. 共价化合物中只含共价键
D. 1H、2H、3H互为同素异形体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示。下列有关说法正确的是

A. 隔膜为阴离子交换膜
B. 电池的电解液可为硫酸
C. 充电时阳极反应为H2O+M+e-=MH+OH-
D. 放电时负极反应为Ni(OH)2+OH—-e-==NiOOH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A. 该装置将化学能转化为电能
B. 为了增加灯泡亮度,可以将电极碳棒变得粗糙多孔
C. 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a
D. 该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数如下表:
MnO2 时间 H2O2 | 0.1 g | 0.3 g | 0.8 g |
10 mL 1.5% | 223 s | 67 s | 56 s |
10 mL 3.0% | 308 s | 109 s | 98 s |
10 mL 4.5% | 395 s | 149 s | 116 s |
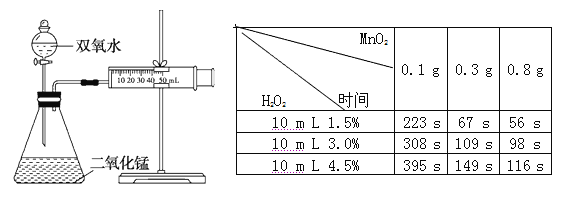
请回答下列问题:
(1)盛装双氧水的化学仪器名称是 。
(2)如何检验该套装置的气密性: 。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而_______(填“加快”或“减慢”或“不变”)。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g(填“ 0.1 g”或“ 0.3 g”或“ 0.8 g”) 的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确___________(填“正确”或“ 不正确”),理由是___________________________。(提示:H2O2的密度可认为近似相等)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是

A.上述电池分别属于一次电池、二次电池和燃料电池
B.干电池在长时间使用后,锌筒被破坏
C.铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D.氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3—CH=CH—Cl,该有机物能发生①取代反应②加成反应③消去反应④使溴水褪色⑤使酸性KMnO4溶液褪色⑥与AgNO3溶液生成白色沉淀⑦聚合反应
A. 以上反应均可发生 B. 只有⑦不能发生
C. 只有⑥不能发生 D. 只有②不能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com