
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:Cu(s)+2H+(aq)![]() Cu2+(aq)+H2(g) ΔH=64 kJ/mol
Cu2+(aq)+H2(g) ΔH=64 kJ/mol
2H2O2(l)![]() 2H2O(l)+O2(g) ΔH=-196 kJ/mol
2H2O(l)+O2(g) ΔH=-196 kJ/mol
H2(g)+![]() O2(g)
O2(g)![]() H2O(l) ΔH=-286 kJ/mol
H2O(l) ΔH=-286 kJ/mol
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为________.
(2)控制其他条件相同,印刷电路板的金属粉末用10% H2O2和3.0 mol/L的H2SO4混合溶液处理,测得不同温度下铜的平均溶解速率(见下表).
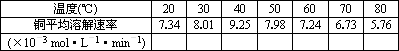
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是________.
(3)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是________.
科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 原子最外层电子数是次外层的三倍 |
| Z | 单质及其化合物的焰色反应为黄色 |
| W | W元素基态原子的M层全充满,N层只有一个电子 |
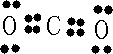
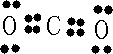
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com