
【题目】PT(KHC2O4·H2C2O4·2H2O,名称:四草酸钾)是一种分析试剂。室温时,H2C2O4的pKa1、pKa2分别为1.23、4.19(pKa=-lgKa)。下列说法不正确的是( )
A.0.1mol·L-1PT溶液中:c(HC2O![]() )>c(K+)>c(H2C2O4)
)>c(K+)>c(H2C2O4)
B.0.1mol·L-1PT中滴加NaOH至溶液pH=4.19:c(C2O![]() )=c(HC2O
)=c(HC2O![]() )
)
C.0.1mol·L-1PT中滴加NaOH至溶液呈中性:c(K+)>c(Na+)>c(HC2O![]() )>c(C2O
)>c(C2O![]() )
)
D.0.1mol·L-1PT与0.1mol·L-1KOH溶液等体积混合,溶液中水的电离程度比纯水的大
【答案】CD
【解析】
A.H2C2O4的第一步电离程度大于第二步电离程度,钾离子不电离也不水解,且![]() ,则
,则![]() 水解平衡常数Kh=
水解平衡常数Kh=![]() <Ka1,说明
<Ka1,说明![]() 的电离程度大于
的电离程度大于![]() 水解程度,所以c(
水解程度,所以c(![]() )>c(K+)>c(H2C2O4),故A正确;
)>c(K+)>c(H2C2O4),故A正确;
B.Ka2=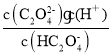 =104.19,0.1molL1PT中滴加NaOH至溶液pH=4.19,则c(
=104.19,0.1molL1PT中滴加NaOH至溶液pH=4.19,则c(![]() )=
)=![]() ,故B正确;
,故B正确;
C.![]() 水解平衡常数Kh=
水解平衡常数Kh=![]() <Ka2,说明
<Ka2,说明![]() 的电离程度大于水解程度导致溶液呈酸性,要使混合溶液呈中性,则加入的n(NaOH)大于n(KHC2O4H2C2O42H2O),则c(K+)<c(Na+),故C错误;
的电离程度大于水解程度导致溶液呈酸性,要使混合溶液呈中性,则加入的n(NaOH)大于n(KHC2O4H2C2O42H2O),则c(K+)<c(Na+),故C错误;
D.0.1molL1PT与0.1molL1KOH溶液等体积混合,二者恰好完全反应生成KHC2O4,因![]() 的电离程度大于水解程度导致溶液呈酸性,其对水的电离的抑制作用大于促进作用,所以其溶液中水的电离程度小于纯水,故D错误;
的电离程度大于水解程度导致溶液呈酸性,其对水的电离的抑制作用大于促进作用,所以其溶液中水的电离程度小于纯水,故D错误;
故选:CD。


科目:高中化学 来源: 题型:
【题目】我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示,下列有关金丝桃素的说法错误的是( )

①属于烃的衍生物,燃烧产物只有CO2和H2O
②可以发生取代、加成、酯化、消去等反应
③分子式为C17H23O3N,苯环上的一氯取代物有3种
④1mol该物质最多能和6molH2发生加成反应
A.①④B.②③C.①③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W原子序数依次增大,A、B、C、D、E为其中两种元素组成的常见化合物,基态Z原子核外有两个未成对电子,A、D均含有10个电子且中心原子的杂化方式相同,它们之间的转化关系如图所示(部分反应物或生成物省略),下列说法中不正确的是( )
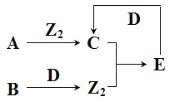
A.简单离子半径:Y>Z>W
B.若C中混有E可用水洗方法除去
C.每个D分子周围可以形成4个氢键
D.B与D反应生成Z2时,D作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,100mL0.1mol·L-1的H2A溶液中滴加0.1mol·L-1NaOH溶液,含A元素相关微粒物质的量随pH的变化如图所示。下列说法正确的是( )
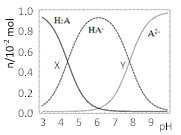
A.将等浓度等体积的Na2A与H2A溶液混合后,溶液显碱性
B.X点所加NaOH溶液体积为50mL
C.X点溶液中含A元素的相关离子存在以下关系:c(H2A)+c(HA-)+c(A2-)=0.1mol·L-1
D.Y点溶液中存在以下关系:c(H+)+c(Na+)=c(OH-)+3c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、H为八种短周期主族元素,原子序数依次增大。A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、H在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17。D与F同周期。G的单质常用作半导体材料。请回答:
(1)C和H分别与A形成的简单化合物沸点较高的是________(填化学式),理由是_____________。
(2)C、E形成的简单离子半径大小:r(C)______r(E)(填>、<或=)
(3)请写出F最高价氧化物对应的水化物在水溶液中的电离方程式______________。
(4)B与G形成的化合物常用于做耐高温材料,工业可用碳热还原法制取:将G的氧化物与B的单质在1400℃条件下和足量的碳反应,请写出化学反应方程式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数,下列说法不正确的是( )
A.标准状况下,22.4 L氦气中含2NA个氦原子
B.18g水中含有的电子数为10NA
C.1mol Cl2与金属Na完全反应,可以得到2NA个电子
D.在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是β—氨基酮类化合物。利用Michael加成反应合成I的路线如图,回答下列问题:
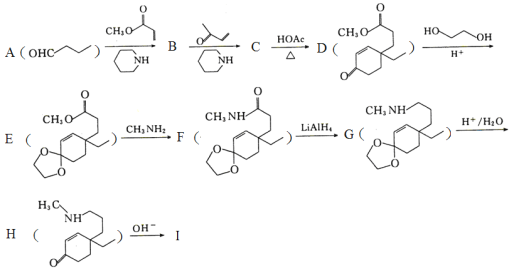
已知:①Michael加成反应通式为:A—CH2—R+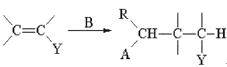 (A,Y可以是CHO、C=O、COOR等;B可以是OH—、CH3CH2O—、
(A,Y可以是CHO、C=O、COOR等;B可以是OH—、CH3CH2O—、![]() 等)
等)
②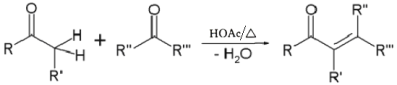
(1)A→B的化学方程式为___。
(2)化合物C和I的结构简式分别为___、___。
(3)B→C和E→F的反应类型分别是___、___。
(4)写出符合下列条件的D的同分异构体的结构简式___。
①与氢氧化钠完全反应时,二者物质的量之比为1:2;
②有4种不同化学环境的氢;
③能使FeCl3溶液显紫色。
(5)写出以苯甲醛、丙酸甲酯和![]() 为原料合成
为原料合成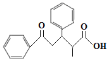 的合成路线___(其它试剂任选)
的合成路线___(其它试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬![]() 在溶液中主要以
在溶液中主要以![]() 蓝紫色
蓝紫色![]() 、
、![]() 绿色
绿色![]() 、
、![]() 橙红色
橙红色![]() 、
、![]() 黄色
黄色![]() 等形式存在,
等形式存在,![]() 为难溶于水的灰蓝色固体,回答下列问题:
为难溶于水的灰蓝色固体,回答下列问题:
(1)![]() 与
与![]() 的化学性质相似,在
的化学性质相似,在![]() 溶液中逐滴加入NaOH溶液直至过量,可察到的现象是 ______________________________________________ .
溶液中逐滴加入NaOH溶液直至过量,可察到的现象是 ______________________________________________ .
(2)![]() 和
和![]() 在溶液中可相互转化
在溶液中可相互转化![]() 室温下,初始浓度为
室温下,初始浓度为![]() 的
的![]() 溶液中
溶液中![]() 随
随![]() 的变化如图所示.
的变化如图所示.

![]() 用离子方程式表示
用离子方程式表示![]() 溶液中的转化反应______________________________ .
溶液中的转化反应______________________________ .
![]() 由图可知,溶液酸性增大,
由图可知,溶液酸性增大,![]() 的平衡转化率__________________
的平衡转化率__________________ ![]() 填“增大“减 小”或“不变”
填“增大“减 小”或“不变”![]() 根据A点数据,计算出该转化反应的平衡常数为 _______________ .
根据A点数据,计算出该转化反应的平衡常数为 _______________ .
![]() 升高温度,溶液中
升高温度,溶液中![]() 的平衡转化率减小,则该反应的
的平衡转化率减小,则该反应的![]() ______
______ ![]() 填“大于”“小于”或“等于”
填“大于”“小于”或“等于”![]() .
.
(3)在化学分析中采用![]() 为指示剂,以
为指示剂,以![]() 标准溶液滴定溶液中的
标准溶液滴定溶液中的![]() ,利用
,利用![]() 与
与![]() 生成砖红色沉淀,指示到达滴定终点
生成砖红色沉淀,指示到达滴定终点![]() 当溶液中
当溶液中![]() 恰好完全沉淀
恰好完全沉淀![]() 浓度等于
浓度等于![]() 时,溶液中
时,溶液中![]() 为 ______
为 ______ ![]() ,此时溶液中
,此时溶液中![]() 等于 ______
等于 ______ ![]() 已知
已知![]() 、AgCl的
、AgCl的![]() 分别为
分别为![]() 和
和![]()
(4)![]() 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用![]() 将废液中的
将废液中的![]() 还原成
还原成![]() ,反应的离子方程式为 _________________________________________________ .
,反应的离子方程式为 _________________________________________________ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com