
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 1H和2H是不同的核素,它们的质子数相等 | |
| C. | ${\;}_{90}^{230}$Th与${\;}_{90}^{232}$Th互为同素异形体 | |
| D. | ${\;}_{1}^{1}$ H、${\;}_{1}^{2}$ H、${\;}_{1}^{3}$ H、H+、H2是氢元素的五种不同粒子 |
分析 A.质子数相同中子数不同的同种元素的不同原子为同位素;
B.原子符号左下角为质子数,左上角为质量数;
C.同种元素组成的不同单质为同素异形体;
D.微粒指的是原子、分子和离子,11H、12H、13H是氢元素的三种不同原子为氢元素的同位素,H+是氢元素的离子,H2是氢元素的分子.
解答 解:A.13C和14C质子数相同属于同一种元素,质量数不同中子数不同为同位素,故A正确;
B.1H和2H是不同的核素,它们的质子数相等都为1,故B正确;
C.${\;}_{90}^{230}$Th与${\;}_{90}^{232}$Th不是单质,是元素的原子互为同位素,故C错误;
D.11H、12H、13H是氢元素的三种不同原子,H+表示氢离子,H2表示氢气分子,是氢元素的五种不同粒子,故D正确;
故选C.
点评 本题主要考查的是同位素、同素异形体的概念和元素性质,题目难度不大,注意区别这两个概念.


科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦ | B. | ②③④⑤ | C. | ③④⑥⑦ | D. | ①③⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
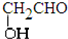 ③CH3CH2CH2CH3和
③CH3CH2CH2CH3和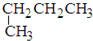
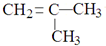 ⑥
⑥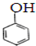 和
和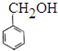
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氧化剂是C12 | B. | 每有1mol C12反应转移1mole- | ||
| C. | 反应中S元素的价态降低 | D. | 该反应中H2O被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
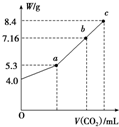 钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠,这些物质在实际生活中有广泛的应用,在一定条件下相互间能进行转化.
钠有多种化合物,如氧化钠、过氧化钠、氢氧化钠、碳酸钠、碳酸氢钠,这些物质在实际生活中有广泛的应用,在一定条件下相互间能进行转化.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成原电池的正极和负极必须是两种不同的金属 | |
| B. | 任何化学反应只要是自发进行的放热反应都可以被设计成原电池 | |
| C. | 在原电池中,电子流出的一极是负极,该电极被还原 | |
| D. | 原电池是化学能转变为电能的装置,为外界提供电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com