
有A.B.C.D.E五种微粒:
①A微粒核内有14个中子,核外M电子层上有2个电子;
②B微粒得到2个电子后,其电子层结构与Ne相同;
③C微粒带有一个单位的正电荷,核电荷数为11;
④D微粒核外有18个电子,当失去1个电子时呈电中性;
⑤E微粒不带电,其质量数为1。
依次写出A.B.C.D.E各微粒的符号
、 、 、 、 ;
科目:高中化学 来源: 题型:
| 元素编号 | A | B | C | D | E |
| X | 3.5 | 3.0 | X3 | 1.5 | 1.5 |
| 主要化合价 | -2 | +7 | +6 | +3 | +2 |


查看答案和解析>>
科目:高中化学 来源: 题型:
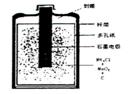 某学校设计了一节实验活动课,让学生从废
某学校设计了一节实验活动课,让学生从废
旧干电池回收碳棒、锌皮、![]() 、
、![]() 、
、![]() 等物质,
等物质,
整个实验过程如下,请回答有关问题。
(1)有关干电池的基本构造和工作原理。右图是干电池的
基本构造图。干电池工作时负极上的电极反应式子是 ,![]()
的作用是除去正极上的产物,本身生成Mn2O3,该反应的化学方程式是 。
锌皮和碳棒的回收。用钳子和剪子开回收的干电池的锌筒,将锌皮和碳棒取出,并用手刷刷洗干净,将电池内的黑色粉末移入小烧杯中。
氧化铵、氯化锌的提取、检验和分离。
如何从黑色粉末中提取![]() 和
和![]() 等晶体的混合物?写出简要的实验步骤。
等晶体的混合物?写出简要的实验步骤。
设计简单的实验证明所得晶体中含有![]() 和
和![]() [一直
[一直![]() 是两性氢氧化物且溶解于氨水],并且填写下列实验报告。
是两性氢氧化物且溶解于氨水],并且填写下列实验报告。
| 实验步骤 | 实验现象 | 实验结论 | 有关离子方程式 |
| (a) | |||
| (b) | (c) | 说明有 | (d) |
| (e) | (f) | 说明有 |
(a) ,(b) ,(c) ,(d) ,(e) ,(f) ,
(4)最后剩余的黑色残渣的主要成分是![]() ,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中需要用到的主要仪器除酒精灯外有(写其中2中即可) 。
,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中需要用到的主要仪器除酒精灯外有(写其中2中即可) 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省雅安中学高一4月月考化学试卷(带解析) 题型:填空题
有A,B,C,D,E五种短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素.金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍.D的气态氢化物的水溶液呈碱性,而其最高价氧化物的水化物为强酸,E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个.
(1)写出元素名称:A. B. C. D . E. .
(2)写出C1,C2, C3粒子的符号: , ,
(3)写出E离子的结构示意图 E的氢化物的分子式 .
(4)写出A的单质与B的单质反应的化学方程式 ;
(5)写出A的单质和B的单质分别与水反应的化学方程式 , ,将二者反应后生成的溶液混合,发生反应的离子方程式为
(6)A与C形成的化合物中含化学键类型是 .用电子式表示该化合物的形成过程 .
查看答案和解析>>
科目:高中化学 来源:2015届四川省高一4月月考化学试卷(解析版) 题型:填空题
有A,B,C,D,E五种短周期元素,A与B可形成BA型化合物,且A元素是非金属性最强的元素.金属B的原子核内质子数比它前一周期同主族元素原子的质子数多8个;C元素有三种同位素C1,C2,C3,自然界里含最多的是C1,C3的质量数是C1的3倍,C2的原子的质量数是C1的2倍.D的气态氢化物的水溶液呈碱性,而其最高价氧化物的水化物为强酸,E元素原子的最外层电子数比次外层电子数多4个,E离子的核外电子数比质子数多2个.
(1)写出元素名称:A. B. C. D . E. .
(2)写出C1,C2, C3粒子的符号: , ,
(3)写出E离子的结构示意图 E的氢化物的分子式 .
(4)写出A的单质与B的单质反应的化学方程式 ;
(5)写出A的单质和B的单质分别与水反应的化学方程式 , ,将二者反应后生成的溶液混合,发生反应的离子方程式为
(6)A与C形成的化合物中含化学键类型是 .用电子式表示该化合物的形成过程 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com