
联合国气候变化大会于2009年12月7-18日在哥本哈根召开。中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40 %~45 %。
(1)有效“减碳”的手段之一是节能。下列制氢方法最节能的是 。(填字母序号)
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O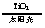 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O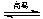 CO+3H2
CO+3H2
 (2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:
(2)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,
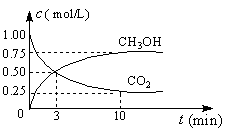
测得CO2和CH3OH(g)的浓度随时间变化如右图所示。
①写出由CO2和H2制取甲醇的反应的平衡常数
表达式 _
②从3 min到10 min,v(H2)= mol/(L·min)。
③能说明上述反应达到平衡状态的是 (填选项编号)
A.反应中CO2和CH3OH的物质的量浓度之比为1:1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗3molH2,同时生成1molH2O
D.CO2的体积分数在混合气体中保持不变
④下列措施能使n(CH3OH)/(CO2)增大的是 (填选项编号)
A.升高温度 B.恒温恒容充入氦气
C.将水蒸气从体系中分离 D.恒温恒容再充入1 mol CO2和3 mol H2
(3)CO2加氢合成DME(二甲醚)是解决能源危机的研究方向之一。
2 CO2(g)+ 6H2(g)→ CH3OCH3(g)+3H2O(l)。有人设想利用二甲醚制作燃料电池,以KOH溶液做电解质溶液,试写出该电池工作时负极反应的电极反应方程式 。
科目:高中化学 来源: 题型:
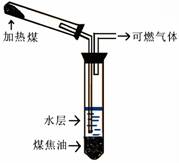
煤的干馏实验如图所示:
(一)水层中溶有铵盐、氨,可以作为化工原料
(1)下列方法中,不能用于实验室制取氨的是( )
A.在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
B.加热试管中的氯化铵固体
C.将烧瓶中的浓氨水加热
D.将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
(二)可燃气体被称为焦炉气,含有甲烷、乙烯、CO、氢气。
(2)检验焦炉气中是否含有乙烯应加入的化学试剂 ;
(3)CO有毒,汽车尾气中也含有CO,同时含有的NO也是一种污染物,汽车燃料中不含氮元素,那么NO是如何产生的?请用化学方程式说明 。
治理汽车尾气中CO、NO的一种方法是:在排气管安装催化转化装置,使NO、CO反应生成无污染的气体,化学方程式为 。
(三)煤焦油中有苯、甲苯、二甲苯、酚类
(4)酚类和醇类的官能团都是羟基,常见的醇类物质为乙醇,向盛有乙醇的烧杯里投入一小块金属钠,可以观察到的现象是( )
A.钠块沉在乙醇液面以下 B.钠块熔成小球
C.钠块在乙醇液面上游动 D.钠块表面有气泡产生
(四)干馏剩余的固体物质主要是焦炭,可以用于冶金、合成氨造气、电石、燃料。
(5)例如:以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:
①在高温下,向金红石与焦炭的混合物中通入氯气,得到TiCl4和一种可燃性气体;
②在稀有气体(如Ar)氛围和加热条件下,用Mg与TiCl4反应可以得到的钛。写出两步的方程式。
。 。
(五)煤的干馏需要隔绝空气加强热,而实验室中用于灼烧或熔融固体物质的常用仪器是坩埚,其材质种类很多,实验时应根据物质的性质加以选择。熔融烧碱时,不能使用普通的玻璃坩埚、石英坩埚和陶瓷坩埚,可以使用 (填材料名称)坩埚。
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。
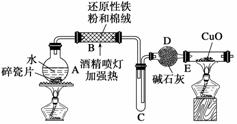
(1)硬质玻璃管B中发生反应的化学方程式为_________________________________
________________________________________________________________________。
(2)反应前A中投放碎瓷片的目的是________________________________________。
(3)装置E中的现象是_____________________________________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________后,将所得溶液分成两份。
(5)一份滴加几滴KSCN溶液。若溶液变血红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为________。
①一定有Fe3O4 ②一定有Fe
③只有Fe3O4 ④只有Fe
(6)另一份用______________(填仪器名称)加入________,可以证明溶液中存在Fe2+。
探究三 设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。
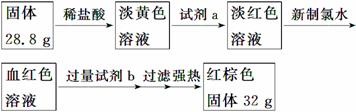
(7)试剂b的化学式是________。
(8)计算反应后B装置中铁元素的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是:
A.氯水中有平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
B.对CO(g)+NO2(g)  CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
C.升高温度能够促进水的电离
D.SO2催化氧化成SO3的反应,往往加入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中有关物质的量浓度关系和计算不正确的是:
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl)
B.已知25°C时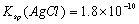 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质的量浓度最大可达到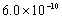 mol·L-1
mol·L-1
C.0.2mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有C(HA-) >C(H+)>C(A2-)>C(H2A)
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,设计正确且能达到实验目的的是[微软用户5]
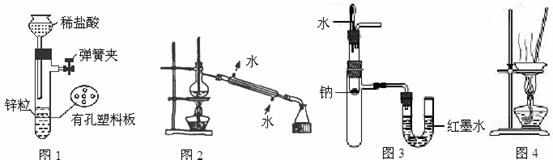
A.用图1所示装置制取少量H2
B.用图2所示装置分离Na2CO3溶液和CH3COOC2H5的混合物
C.用图3所示装置验证Na和水反应的热效应
D.用图4所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
胡妥油(D)用作香料的原料,它可由A合成得到:
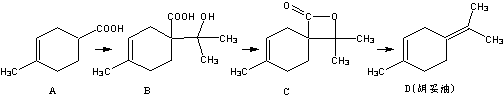
下列说法正确的是[微软用户12]
A.若有机物A是由异戊二烯(C5H8)和丙烯酸(C3H4O2)加热得到的,则该反应的反应类型属于加成反应
B.有机物D分子中所有碳原子一定共面
C.有机物C 的所有同分异构体中不可有芳香族化合物存在
D.有机物B 既能跟Na反应放出H2,又能跟NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
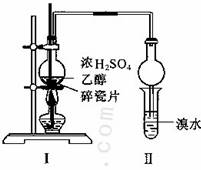 l,2二溴乙烷可作汽油抗爆剂的添加剂,常温 下它是无色液体,密度2.189.cm
l,2二溴乙烷可作汽油抗爆剂的添加剂,常温 下它是无色液体,密度2.189.cm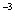 ,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在 实验室中可用下列反应制备1,2二溴乙烷。
,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在 实验室中可用下列反应制备1,2二溴乙烷。

某化学兴趣小组用如图所示的装置(部分固定和夹持装置省略)进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
回答下列问题:
(1)已知该实验的副反应之一是乙醇会被浓硫酸氧化成CO2。写出该反应的化学方程式:
_________________________________________________________________。
(2)甲同学认为:溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理
由是________(填正确答案的标号,下同)。
A.乙烯与溴水易发生取代反应 B.使溴水褪色的物质,未必是乙烯
C.使溴水褪色的反应,未必是加成反应
D.浓硫酸氧化乙醇生成的乙醛,也会使溴水褪色
(3)乙同学经过仔细观察后认为试管中另一现象可证明反应中有乙烯生成,该现象是
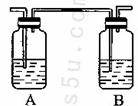 (4)丙同学对上述实验进行了改进,在I和II之间增加如图所示的装置,则A中的试剂为________,其作用是________B中的试剂为________,其作用是________。
(4)丙同学对上述实验进行了改进,在I和II之间增加如图所示的装置,则A中的试剂为________,其作用是________B中的试剂为________,其作用是________。
(5)丁同学通过洗涤、蒸馏等操作对l,2一二溴乙烷粗品进行了精制。该洗涤操作用到的主要玻璃仪器是_________,该仪器在使用前须清洗干净并_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com