
【题目】最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4气态分子。N4分子结构如图所示,已知断裂1molN-N吸收l67KJ的热量,生成lmol N![]() N放出942KJ热量。
N放出942KJ热量。
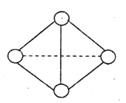
(1)试写出由N4气态分子变成N2气态分子的热化学方程式:_____________________。
(2)某盐N2H6Cl2的性质与NH4Cl类似,是离子化合物,其水溶液因分步水解而呈弱酸性。
①N2H6Cl2显酸性原因(用离子方程式表示)__________________________。
②写出足量金属镁加入盐N2H6Cl2的溶液中产生H2的化学方程式为____________________。
【答案】 N4(g)=2N2(g)△H=-882kJ/mol N2H62++H2O![]() [N2H5
[N2H5![]() H2O]++H+ Mg+N2H6Cl2=MgCl2+N2H4+H2↑
H2O]++H+ Mg+N2H6Cl2=MgCl2+N2H4+H2↑
【解析】试题分析:(1)根据焓变=反应物的总键能-生成物的总键能计算N4气态分子变成N2气态分子的焓变;(2)N2H6Cl2的性质与NH4F类似,根据铵根离子水解方程式,写N2H62+水解的离子方程式;②根据氯化铵与金属镁反应生成氯化镁、氨气和氢气,足量金属镁加入盐N2H6Cl2的溶液中产生H2、氯化镁、N2H4;
解析:(1)根据焓变=反应物的总键能-生成物的总键能,发生反应N4=2N2,△H=6×167kJ/mol-2×942kJ/mol=-882kJ/mol,所以反应的热化学方程式是N4(g)=2N2(g) △H=-882kJ/mol;
(2)①根据铵根离子水解方程式,盐N2H6Cl2显酸性原因:N2H62++H2O![]() [N2H5
[N2H5![]() H2O]++H+。
H2O]++H+。
②足量金属镁加入盐N2H6Cl2的溶液中产生H2、氯化镁、N2H4,反应化学方程式为
Mg+N2H6Cl2=MgCl2+N2H4+H2↑


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:高中化学 来源: 题型:
【题目】已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10,现向1 L 0.2 mol·L-1HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中,正确的是
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. Ksp(CaF2)随温度和浓度的变化而变化
C. 该体系中没有沉淀产生
D. 该体系中HF与CaCl2反应产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Ag+ Na+ |
阴离子 | NO3- SO42- Cl- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A、 B、 C三种溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加了27g。常温下各烧杯中溶液的pH与电解时间(t)的关系如图。据此回答下列问题:

(1)M为电源的__________极(填“正”或“负”)。
(2)写出甲烧杯中反应的化学方程式____________________。
(3)有人设想用图一所示原电池为直流电源完成上述电解。则锌电极相当于直流电源的_________(填“M”或“N”)极。

(4)有人设想用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。该设想中负极的电极反应式为 __________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生物电化学方法脱除水体中NH4+的原理如下图所示:
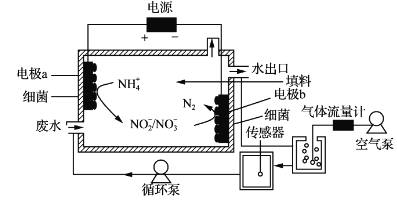
下列说法正确的是
A. 装置工作时,化学能转变为电能
B. 装置工作时,a极周围溶液pH降低
C. 装置内工作温度越高。NH4+脱除率一定越大
D. 电极b上发生的反应之一是:2NO3--2e-=N2↑+3O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸米多君是临床常用的升压药,其一种合成路线如下:

(1)盐酸米多君中含氧官能团名称为_____________(只写两种)。
(2)B→C的反应类型为___________。
(3)写出满足下列条件的B的一种同分异构体的结构简式:_______。
①含有苯环,分子中有一个手性碳原子,能发生银镜反应,与FeCl3溶液发生显色反应,在酸性条件下水解可生成两种有机物。
②分子中只有5种不同化学环境的氢。
(4)E的分子式为C10H15O3N,经取代得到F。写出E的结构简式:_______。
(5)已知:![]() ,请写出以
,请写出以![]() 和
和![]() 为原料制备
为原料制备![]() 的合成路线流程图______(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图______(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】易混易错题组
物质在水中可能存在电离平衡、盐类的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学的知识回答:
(1)A为0.1 molL-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为________________________________________________。
(2)B为0.1 molL-1 NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(共3个,分别用离子方程式表示):_____________________________________________
(3)C为Al2(SO4)3溶液,实验室中配制Al2(SO4)3溶液时通常需要向其中加入_______________,若把B和C溶液混合,将产生白色沉淀和无色气体,该反应的离子方程式为___________________。
(4)pH=2的某酸HnA(An-为酸根)与pH=12的某碱B(OH)m混合,恰好反应生成正盐,混合液pH=8,反应生成的正盐的化学式为_________,盐中________离子一定能水解,其第一步水解的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是
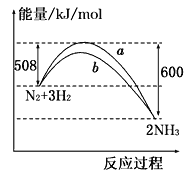
A. 该反应的热化学方程式为:N2 + 3H2 ![]() 2NH3, △H = -92kJ·mol-1
2NH3, △H = -92kJ·mol-1
B. 在温度体积一定的条件下, 通入lmol N2和3molH2反应后放出的热量为92kJ
C. b曲线是加入催化剂时的能量变化曲线
D. 加入催化剂, 该化学反应的ΔH不改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如右。下列说法不正确的是

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及极性键的断裂与生成
C. 氧化剂与还原剂的物质的量之比为1∶3
D. 原料气N2可通过分离液态空气获得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com