
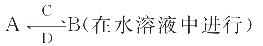
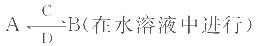 其中C是溶于水显酸性的气体;D是淡黄色固体。则C为CO2,D为Na2O2,二者反应的化学方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;①B为两性不溶物,结合转化关系可知,A为四羟基合铝酸钠、B为氢氧化铝,四羟基合铝酸根与二氧化碳反应生成氢氧化铝,反应离子方程式为:[Al(OH)4]-+CO2 = Al(OH)3↓+ HCO3-;②B由四种元素组成,B溶液显碱性,结合转化关系可知,A为碳酸钠、B为碳酸氢钠,碳酸氢钠在化学键类型为离子键、共价键;碳酸钠属于盐。
其中C是溶于水显酸性的气体;D是淡黄色固体。则C为CO2,D为Na2O2,二者反应的化学方程式为:2Na2O2 + 2CO2 = 2Na2CO3 + O2;①B为两性不溶物,结合转化关系可知,A为四羟基合铝酸钠、B为氢氧化铝,四羟基合铝酸根与二氧化碳反应生成氢氧化铝,反应离子方程式为:[Al(OH)4]-+CO2 = Al(OH)3↓+ HCO3-;②B由四种元素组成,B溶液显碱性,结合转化关系可知,A为碳酸钠、B为碳酸氢钠,碳酸氢钠在化学键类型为离子键、共价键;碳酸钠属于盐。

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应 |
| B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键 |
| C.丙中含有第二周期IV A族的元素,则丙一定是甲烷的同系物 |
| D.丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.属于金属元素 | B.质子数与中子数之差为50 |
| C.原子的核外电子数是39 | D.8939Y和9039Y是两种不同的核素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
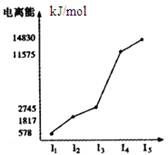
| A.X元素显+4价 |
| B.X为非金属 |
| C.X为第五周期元素 |
| D.X与氯反应时最可能生成的阳离子为X3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
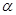 粒子轰击极簿的金箔。为了解释实验结果,提出了原子的核式结构学说。下列图中,黑点表示金原子核的位置,曲线ab、cd和ef表示经过金原子核附近的
粒子轰击极簿的金箔。为了解释实验结果,提出了原子的核式结构学说。下列图中,黑点表示金原子核的位置,曲线ab、cd和ef表示经过金原子核附近的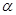 粒子的运动轨迹,能正确反映实验结果的图是( )
粒子的运动轨迹,能正确反映实验结果的图是( )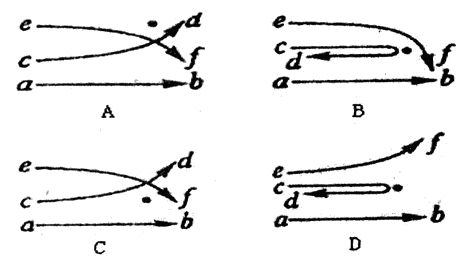
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com