
| A. | 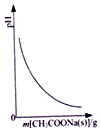 图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 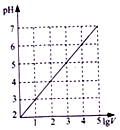 图表示0.1LpH=2的HC1溶液加水稀释至VL,pH随lgV的变化 | |
| C. | 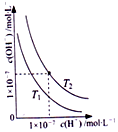 图表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1 | |
| D. | 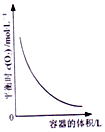 图表示同一温度下,再不同容积的容器中进行反应2BaO2(s)?2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系 |
分析 A.醋酸溶液中存在电离平衡,加入醋酸钠,醋酸根离子浓度增大抑制醋酸电离,溶液中氢离子浓度减小;
B.盐酸是强酸溶液,加水稀释10n倍,溶液的pH变化增大n个单位,但只能接近;
C.图象分析可知,T1温度下,氢离子浓度和氢氧根离子浓度乘积小于T2温度下氢离子浓度和氢氧根离子浓度乘积,水的电离是吸热过程,温度越高水电离程度越大,氢离子和氢氧根离子浓度乘积越大,据此分析;
D.同一温度下,在不同容积的容器中进行反应2BaO2(s)?2BaO(s)+O2(g),体积越大压强越小,则平衡正向进行,氧气浓度增大,但体积增大引起的浓度减小,相同温度下平衡常数不变,此反应的平衡常数K=c(O2);
解答 解:A.醋酸溶液中存在电离平衡,加入醋酸钠,醋酸根离子浓度增大抑制醋酸电离,溶液中氢离子浓度减小,溶液PH增大,图象不符合,故A错误;
B.盐酸是强酸溶液,加水稀释10n倍,溶液的pH变化增大n个单位,但只能接近7,不能等于7,故B错误;
C.升温促进水电离,Kw增大,水电离的氢离子浓度增大,所以氢离子浓度大的温度高,即温度T2>T1,故C正确;
D.增大容器的体积,氧气的浓度减小,平衡向正方向移动,氧气的物质的量增大,氧气的浓度先增大,当达到平衡状态时浓度增大,然后随着体积的增大浓度减小,温度不变,平衡常数不变,K=c(O2),最终氧气平衡浓度不变,则图象不符,故D错误.
故选C.
点评 本题考查了弱酸的电离、影响水的电离平衡的因素、化学平衡移动等,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力,注意把握有关的反应原理以及影响平衡的条件.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| B. | 加入水,平衡向逆反应方向移动 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,溶液中C(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ─484 kJ•mol-1 | B. | +484 kJ•mol-1 | C. | ─242 kJ•mol-1 | D. | +242 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲醇的结构式:CH4O | |
| B. | 钠离子的结构示意图: | |
| C. | 质子数为16、中子数为17的硫原子:${\;}_{16}^{17}$S | |
| D. | 硫化氢分子的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 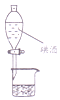 用图装置分离该酒中的碘和酒精 | B. | 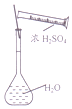 用图装置配制稀硫酸 | ||
| C. |  用图装置由食盐水制得食盐晶体 | D. | 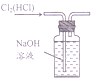 用图装置除去Cl2中的HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯分子中含有碳碳双键 | B. | 氨基酸分子中可能含有手性碳原子 | ||
| C. | 己烷有3种同分异构体 | D. | 乙酸分子中所有原子处于同一平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8.0gCH4中含有的氢原子数为NA | |
| B. | 1mol氯气跟水完全反应,转移的电子数为2NA | |
| C. | 1 molNa2O2跟足量CO2完全反应,转移的电子数为NA | |
| D. | 0.1mol/L MgCl2溶液中含氯离子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com