
25 ℃,水的电离达到平衡: H2O H++OH-;H>0,下列叙述正确的是
H++OH-;H>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
科目:高中化学 来源: 题型:
下列事实中不能应用勒夏特列原理来解释的是
A、新制的氯水在光照条件下颜色变浅
B、加入催化剂能使合成氨的速率加快
C、高压对合成氨有利
D、室温比500℃左右更有利于合成氨的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个恒压的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)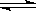 A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
A.平均反应速度:乙>甲 B.平衡时C的物质的量甲>乙
C.平衡时C的转化率:乙<甲 D.平衡时A的物质的量甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和压强下,有如下反应:
2SO2(g)+O2(g)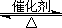 2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L。经一段时间后,反应达到平衡,测得混合气体的体积为80L。请回答下列问题:
2SO3(g),将1.6molSO2和0.8mol的O2放入一体积可变的密闭容器中,测得容器的起始容积为100L。经一段时间后,反应达到平衡,测得混合气体的体积为80L。请回答下列问题:
⑴达平衡时SO2的转化率为 ;
⑵若起始时加入amolSO2、bmolO2,且a︰b=2︰1,在同样温度和压强下,反应达到平衡时,测得混合气体的容积为120L。则a、b的值分别为:a= ,b= ;
⑶若容器为体积不变的密闭容器,其容积为100L。起始时加入xmolSO2、ymolO2和zmolSO3,反应达平衡时,温度和压强与(2)完全相同,容器内各气体的体积分数也与(2)达平衡时的情况完全相同。则x、y应该满足的关系式为 ,x、z应该满足的关系式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液状态下电离方程式错误的是
A.CaCO3 = Ca2++CO32— B.NaHSO4 = Na++HSO4—
C.H2CO3 H++HCO3— D.NH3·H2O
H++HCO3— D.NH3·H2O NH4++OH—
NH4++OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应aA(s)+bB(g) cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是
cC(g) +dD(g), 当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示,据图分析,以下正确的是
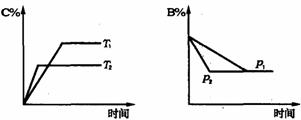 A.T1>T2,正反应放热
A.T1>T2,正反应放热
B.Tl<T2,正反应吸热
C.P1>P2,a+b=c+d
D.Pl<P2,b=c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
100mL6mol·L-1硫酸跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,加入下列物质不能达到实验目的的是
A.硫酸钠(aq) B.硝酸钾(aq) C.醋酸钠(s) D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.104 | 0.111 | 0.066 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
下列叙述正确的是( )
A.L与T形成的化合物属于共价化合物 B.M的最高价氧化物的水化物具有两性
C.T、Q的氢化物常温常压下均为无色气体 D.L、M的单质与稀盐酸反应速率:M>L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )。
A.H2SO4的酸性比HClO的酸性强,所以S的非金属性比Cl强
B.Mg (OH)2是中强碱,Al(OH)3是两性氢氧化物,所以Al比Mg活泼
C.H2S 300℃时开始分解,H2O 1000℃时开始分解,说明O的非金属性比S强
D.Na和Mg与酸都能激烈反应放出氢气,故无法比较它们的金属性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com