
【题目】下列溶液中与50 mL1mol/LAlCl3溶液中Cl-物质的量浓度相等的是
A. 50 mL 1 mol/LFeCl3溶液 B. 75 mL 2mol/LKCl溶液
C. 150 mL 1 mol/LMgCl2溶液 D. 25 mL 3 mol/LCuCl2溶液
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列溶液中粒子的物质的量浓度关系正确的是
A. 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:C(Na+)>c(CO32 -)>c(HCO3- )>c(OH-)
B. CH3COOH溶液加水稀释,溶液中![]() 不变
不变
C. 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-)
D. 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,世界上多采用电解熔融氯化钠的方法来生产金属钠:2NaCl(熔融) ![]() 2Na+Cl2↑。已知A、B、C、D、E有如下转化关系:
2Na+Cl2↑。已知A、B、C、D、E有如下转化关系:
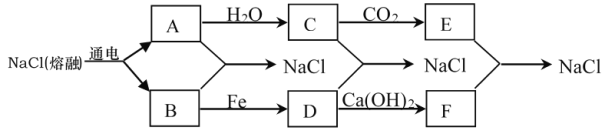
(1)写出A、B生成NaCl的化学方程式:_____________________________________。
(2)写出化学式:C______________,D_____________。
(3)工业生产中常利用B与Ca(OH)2反应来制备漂白粉,漂白粉的主要成分是_______________________________。(写化学式)
(4)若把A投入盛有D的溶液中,溶液中出现________________(填沉淀颜色)沉淀,该过程所发生反应的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于ag H2和bg He 的说法正确的是
A. 同温同压下,H2和He的体积比是a:b
B. 同温同压下,若a=b,则H2与He的物质的量之比是2:1
C. 体积相同时,He 的质量一定大于H2的质量
D. 同温同压下,若二者的物质的量相等,其密度也相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生配制100mL1 mol·L-1的硫酸溶液,进行下列操作,然后对溶液浓度作精确测定,发现真实浓度小于1 mol·L-1,他的下列操作中使浓度偏低的原因是
①用量筒量取浓硫酸时,俯视读数
②量筒中浓硫酸全部转入烧杯中稀释后,再转移到100mL容量瓶中,烧杯未洗涤
③容量瓶没有烘干
④用玻璃棒引流,将溶液转移到容量瓶中时有溶液流到了容量瓶外面
⑤溶液未经冷却即定容
⑥用胶头滴管加蒸馏水时,加入过快而使液面超过了刻度线,立即用滴管吸去多余的水,使溶液凹面刚好与刻度线相切
⑦滴加蒸馏水,使溶液凹面刚好与刻度线相切,盖上瓶塞反复摇匀后,静置,发现液面比刻度线低,再加水至刻度线
⑧定容时仰视读数
A. ①②④⑥⑦⑧ B. ②③④⑤⑥⑦ C. ①②③⑤⑥⑦⑧ D. ①②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】VmLAl2(SO4)3 溶液中含SO42- ag,取V/4mL溶液稀释到4VmL,则稀释后溶液Al3+中的物质的量浓度是
A. 125a/(576V) mol/L B. 125a/(288V)mol/L
C. 125a/(144V )mol/L D. 125a/(96V)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种可溶性盐,它们的阳离子分别可能是Ba2+、Ag+、Na+、Cu2+中的某一种,阴离子分别可能是NO3-、SO42-、Cl-、CO32-中的某一种。
Ⅰ.若把四种盐分别溶解于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色。
Ⅱ.若向实验Ⅰ的四支试管中分别加盐酸,B盐溶液有沉淀产生E,D盐溶液有无色无味气体逸出。
根据实验Ⅰ、Ⅱ回答下列问题:
(1)C的名称为___________;D的化学式为______________。
(2)写出盐酸+B反应的离子方程式__________________,化学方程式与盐酸+D反应具有相同的离子方程式。
(3)将沉淀E过滤并洗涤,如何验证沉淀E已洗涤干净_____________________________。
(4)为检测C盐的一些性质,需配制240 mL 0.2 mol/L NaOH溶液,请回答下列问题:
①经计算,需用托盘天平称量固体NaOH的质量为__________g。
②在配制NaOH溶液时除烧杯、玻璃棒外,还需使用的玻璃仪器有________和_________。
③将NaOH浓溶液先____________,再转移到容量瓶中,否则溶液浓度__________(填“偏高”或“偏低”)。
④配制NaOH溶液时定容的操作:加蒸馏水距离刻度线__________处,改用_________滴加,至_______________与刻度线相切。
⑤取出配制好的溶液150mL,可以中和质量分数为36.5%,密度为1.20g/mL的盐酸的体积为____mL,配制该盐酸需HCl的体积为________mL(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许O2-在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
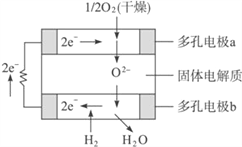
①多孔电极a为负极
②a极对应的电极反应式为O2+2H2O+4e-==4OH-
③b极的电极反应式为H2-2e-+O2-==H2O
④该电池的总反应式为2H2+O2![]() 2H2O
2H2O
A. ①② B. ②④ C. ②③ D. ③ ④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com