
【题目】下面有关Na2CO3与NaHCO3的性质比较中错误的是( )
A. 相同浓度溶液的碱性:Na2CO3>NaHCO3
B. 在水中的溶解度:Na2CO3>NaHCO3
C. 与同浓度的硫酸反应放出气泡的速率:NaHCO3<Na2CO3
D. 热稳定性:NaHCO3<Na2CO3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.钠和冷水反应:Na+2H2O == Na++2OH-+H2↑
B.金属铝溶于氢氧化钠溶液:Al+2OH-== AlO![]() +H2↑
+H2↑
C.金属铝溶于盐酸中:2Al+6H+ == 2Al3++3H2↑
D.铁跟稀硫酸反应:Fe+2H+ == Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应当反应物用量不同时,产物可能不同的是( )
A. 氢氧化钠与碳酸氢钙反应 B. 过氧化钠与二氧化碳反应
C. 单质硫与氧气反应 D. 铁粉与氯气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不锈钢表面用硝酸和氢氟酸的混酸处理后,产生的酸洗废液中含有Fe3+、Ni2+、NO3﹣、F﹣和+6价铬的含氧酸根离子等.如图是综合利用该酸洗废液的工艺流程: 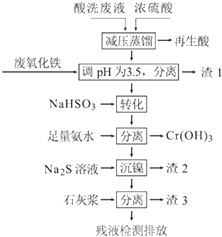
已知:
①金属离子开始沉淀和沉淀完全时的pH:
Fe3+ | Ni2+ | Cr3+ | |
开始沉淀 | 1.5 | 6.7 | 4.0 |
沉淀完全 | 3.4 | 9.5 | 6.9 |
②Ni2+与足量氨水的反应为:Ni2++6NH3[Ni(NH3)6]2+
(1)再生酸中含有 , 采取减压蒸馏的原因是 .
(2)利用废氧化铁(主要成分为Fe2O3)代替烧碱调节pH的好处是 .
(3)请写出“转化”时NaHSO3与Cr2O72﹣发生反应的离子反应方程式: .
(4)已知[Ni(NH3)6]2+为难电离的络合离子,则“沉镍”的离子方程式为: .
(5)滤渣3的主要成分为CaF2、Ca(OH)2和 .
(6)经检测,最后的残液中c(Ca2+)=0.004molL﹣1 , 则残液中F﹣浓度为mgL﹣1 , (填“符合”或“不符合”)排放标准[已知Ksp(CaF2)=4×10﹣11 mol3L﹣3 , 国家排放标准要求氟离子浓度小于10mgL﹣1].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:
达到新的平衡对应的图象 | 平衡移动方向 | |
(i)使用催化剂 | ||
(ii)升温 | ||
(iii)降压 | ||
(iv)增加A的量 | ||
(v)减少C的量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com