
【题目】下列解释事实的离子方程式不正确的是
A. 铝片放入NaOH溶液中有气体产生:2Al + 2OH-+ 2H2O===2AlO2-+3H2↑
B. 向K2Cr2O7溶液中滴加少量浓H2SO4,溶液橙色加深: Cr2O72-(橙色) + H2O![]() 2CrO42-(黄色) + 2H+
2CrO42-(黄色) + 2H+
C. 向Na2SiO3溶液中通入过量CO2制备硅酸凝胶:SiO32-+ CO2 + H2O===H2SiO3(胶体)+ CO32-
D. 用Na2CO3溶液浸泡锅炉水垢(含CaSO4):CaSO4 + CO32-![]() CaCO3 + SO42-
CaCO3 + SO42-
【答案】C
【解析】A. 铝片放入NaOH溶液中有气体产生,发生反应的离子方程式为2Al + 2OH-+ 2H2O===2AlO2-+3H2↑,A正确;B. 向K2Cr2O7溶液中滴加少量浓H2SO4,增大了溶液中的氢离子浓度,可逆反应 Cr2O72-(橙色) + H2O![]() 2CrO42-(黄色) + 2H+形成的化学平衡向逆反应方向移动,溶液橙色加深,B正确;C. 向Na2SiO3溶液中通入过量CO2制备硅酸凝胶,离子方程式为SiO32-+ CO2 + H2O===H2SiO3↓+HCO3-,C不正确;D. 用Na2CO3溶液浸泡锅炉水垢(含CaSO4),硫酸钙可以转化为溶解度更小的碳酸钙,离子方程式为CaSO4 + CO32-
2CrO42-(黄色) + 2H+形成的化学平衡向逆反应方向移动,溶液橙色加深,B正确;C. 向Na2SiO3溶液中通入过量CO2制备硅酸凝胶,离子方程式为SiO32-+ CO2 + H2O===H2SiO3↓+HCO3-,C不正确;D. 用Na2CO3溶液浸泡锅炉水垢(含CaSO4),硫酸钙可以转化为溶解度更小的碳酸钙,离子方程式为CaSO4 + CO32-![]() CaCO3 + SO42-,D正确。本题选C。
CaCO3 + SO42-,D正确。本题选C。


科目:高中化学 来源: 题型:
【题目】规律提炼题组
完成下列与溶液pH有关的计算,并提炼解题规律。
(1)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为_______
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后,溶液中的氢离子浓度为 _____
(3)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:,
①若所得混合溶液为中性,则a:b= ____
②若所得混合溶液pH=3,则a:b=_____
(4)已知某温度时0.1 molL-1NaOH pH等于11,在此温度下,若将100体积pH1=a的H2SO4溶液与1体积pH2=b的NaOH溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是________________(用含a、b的表达式表示)
(5)(学法题)总结归纳求混合溶液pH时,应注意的问题:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示下列描述正确的是

A. 反应开始到10s,用Z表示的反应速率为0.158 mol/(Ls)
B. 反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C. 反应开始到10s,Y的转化率为79.0 %
D. 反应的化学方程式为:X+Y![]() Z
Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如图所示。
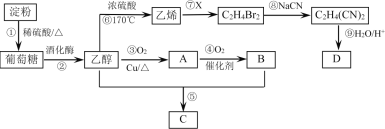
回答下列问题:
(1)淀粉的组成可表示为___________,A分子中的官能团名称为__________。
(2)反应⑦中物质X的分子式为________,反应⑧的类型为______________。
(3)反应⑤的化学方程式为________________________________________________。
(4)反应⑥可用于实验室制乙烯,为除去其中可能混有的SO2,可选用的试剂是________。
A.溴水 B.酸性KMnO4溶液 C. NaOH溶液 D.浓硫酸
(5)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为____________。
(6)为了证明反应①是否发生,可取①反应后的溶液2mL于一支试管中,用____调节溶液至中性,再向其中加入2 mL_____,再加入4~5滴_____(以上用如下所提供试剂的字母填空),加热一段时间,若有______________现象产生,则证明反应①已发生。
实验中可供选择的试剂:
A.10%的NaOH溶液 B.2%的氨水 C.5%的CuSO4溶液 D.碘水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“低碳经济”正成为科学家研究的主要课题。将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g) + 6H2(g) ![]() CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g)
(1) 已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2)/n(CO2)]的变化曲线如下图:
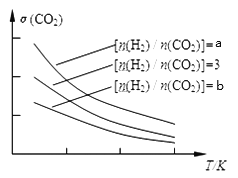
①a、3、b的大小关系___________
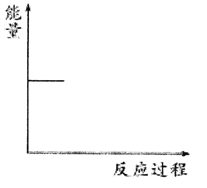
②请根据下图中信息在下图(右)中画出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的能量关系曲线___________。
(2)某温度下,将2.0molCO2(g)和6.0molH2(g)充入容积为2L的密闭容器中,上述反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图所示,关于温度和压强的关系判断正确的______
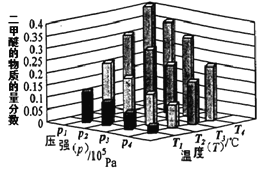
A. P3>P2,T3>T2 B. P1>P3,T1>T3 C. P2>P4,T4>T2 D. P1>P4,T2>T3
(3)在恒容密闭容器里按体积比为1:3充入CO2(g)和H2(g),一定条件下上述反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是___________
A. 正反应速率先增大后减小 B. 逆反应速率先增大后减小
C. 化学平衡常数K值增大 D. 反应物的浓度增大
(4)下列一定能说明上述反应达到平衡的是___________
A.气体的平均摩尔质量不变
B.恒容条件下,气体的密度不变
C.各物质的速率之比等于系数比
D.[n(H2)/n(CO2)]不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列物质分类全部正确的是
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氨 ⑥KClO3
A. 碱①④B. 纯净物③④⑤C. 盐①⑥D. 混合物②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按酸、碱、盐分类顺次排列.正确的( )
A.硫酸,纯碱,孔雀石
B.硝酸,烧碱,绿矾
C.冰醋酸,乙醇,醋酸钠
D.盐酸,熟石灰,苛性钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com