
【题目】有机物W在工业上常用作溶剂和香料,其合成方法如图,下列说法不正确的是

A. M、N、W均能发生加成反应和取代反应
B. N、W组成上相差一个CH2原子团,所以互为同系物
C. 1molM与1molw完全燃烧消耗O2的物质的量相同
D. M苯环上的二氯代物有6种
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Na+、Ca2+、NO、CO![]() 、SO
、SO![]() 、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行以下实验:
、Cl-等离子。为了鉴别这些离子,分别取少量溶液进行以下实验:
①加稀盐酸后,生成无色无味的气体,该气体能使澄清石灰水变浑浊。
②加足量的BaCl2产生白色沉淀,过滤,在沉淀中加入足量的盐酸,沉淀不能完全溶解。
③取②中滤液,加硝酸酸化后,再加过量的AgNO3溶液,析出白色沉淀。
(1)上述3个实验证明一定存在的离子是__________,一定不存在的离子是________,可能存在的离子为_______________。
(2)写出①中涉及反应的离子反应方程式: _____________________________。
(3)实验室中常用于检验Na+是否存在的方法叫___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+ 2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
(1)已知CO(g)、H2(g)的标准燃烧热分别为-285.8kJmol-1,-283.0kJmol-1,且CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) △H=-761 kJmol-1;则CO(g)+ 2H2(g)
CO2(g)+2H2O(l) △H=-761 kJmol-1;则CO(g)+ 2H2(g)![]() CH3OH(g)的△H= ___________。
CH3OH(g)的△H= ___________。
(2)反应的ΔS_______0(填“>”、“<”或“=”)。在________(填“较高”或“较低”)温度下该反应自发进行。
(3)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是_______________。
A.容器内气体密度保持不变 B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与生成H2的速率相等 D.CO的体积分数保持不变
(4)下图中能正确反映平衡常数K随温度变化关系的曲线为__________(用a或b表示)。
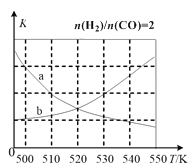
(5)投料比n(H2)/n(CO)=2时,体系中CO的平衡转化率(α)温度和压强的关系如图2所示。α(CO)值随温度升高而___________(填“增大”或“减小”)其原因是___________________________;下图中的压强由大到小为__________________(用P1,P2,P3表示)。

(6)520K时, 投料比n(H2)/n(CO)=2(总物质的量为3mol),维持反应过程中压强P3不变,达到平衡时测得容器体积为0.1L,则平衡常数K=_______。若H2和CO的物质的量之比为n∶1(维持反应过程中压强P3不变),相应平衡体系中CH3OH的物质的量分数为x,请在下图中绘制x随n变化的示意图_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验、现象与结论正确且相符的是( )
实验 | 现象 | 结论 | |
A | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应: 2NO2 (g) |
C | SO2通入新制氯水 | 溶液褪色 | SO2具有漂白性 |
D | 向2支盛有2mL相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液 | 一支无明显现象,另一支产生黄色沉淀 | 相同条件下,AgI比AgCl的溶解度大 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡酸钠用于制造陶瓷电容器的基体、颜料和催化剂。以锡锑渣(主要含Sn、Sb、As、Pb的氧化物)为原料,制备锡酸钠的工艺流程图如下:
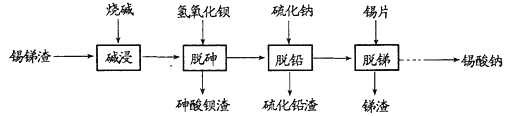
请回答下列问题:
(1)Sn(ⅣA)、As(VA)、Sb(VA)三种元素中,As和Sb最高正化合价为___________,Sn的原子序数为50,其原子结构示意图为___________。
(2)从溶液中得到锡酸钠晶体的实验操作是___________、趁热过滤、干燥。
(3)“碱浸”时,若SnO含量较高,工业上则加入NaNO3,其作用是______________________;如图是“碱浸”实验的参数,请选择“碱浸”的合适条件_________________________________。
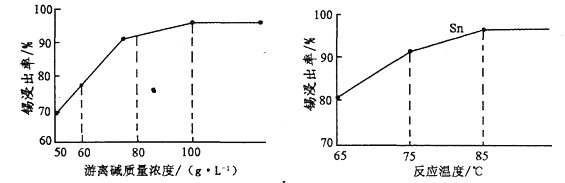
(4)“脱铅”是从含Na2PbO2的溶液中形成硫化铅渣,其离子方程式为_________________。
(5)“脱锑”时发生的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对某溶液中部分离子的定性检测流程如下。相关分析正确的是
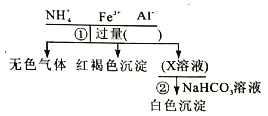
A. 步骤①所加试剂可以是浓KOH溶液
B. 可以用湿润的蓝色石蕊试纸检验生成的无色气体
C. 步骤②的反应为Al3++3HCO3-=A1(OH)3↓+CO2↑
D. 检验Fe3+的离子反应方程式为Fe3++3SCN-=Fe(SCN)3↓(血红色)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是 ( )
A. 同分异构体之间分子式相同,其式量也一定相等,式量相等的物质一定是同分异构体。
B. 同分异构体之间某种元素的质量分数均相同,化合物之间某种元素质量分数均相同的物质一定为同分异构体。
C. 两种物质如果互为同分异构体,则一定不可能为同系物。
D. 互为同分异构体的物质之间物理性质一定不同,但化学性质一定相似。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 等体积pH=2的HX和HY两种酸分别与足量的铁反应,用排水法收集气体 | HX放出的氢气多且反应速率快 | 酸的强弱:HX<HY |
B | 向2 mL 0.1 mol/L Na2S溶液中滴2滴0.1 mol/L ZnSO4溶液;再滴2滴0.1 mol/L CuSO4 | 先生成白色沉淀,后生成黑色沉淀 | 溶度积(Ksp):ZnS>CuS |
C | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+3KSCN |
D | 常温下,用pH计分别测定饱和NaA溶液和饱和NaB溶液的pH | pH:NaA>NaB | 常温下酸性:HA﹤HB |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得25℃、101 kPa时,1 mol甲醇完全燃烧释放726.51kJ的热量,下列热化学方程式书写正确的是( )
A. 2CH3OH+3O2=2CO2+4H2O ΔH=-1453.02 kJ·mol-1
B. 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=+1453.02 kJ·mol-1
C. CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=-726.51 kJ·mol-1
D. CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-726.51 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com