
| A. | 为避免船体遭受腐蚀,在船舶的外壳装上若干锌块,称为牺牲阳极的阴极保护法 | |
| B. | 原电池工作时,电流的方向由正极→负载→负极→原电池中电解质溶液→正极 | |
| C. | 白铁(镀锌铁)镀层破损后,铁皮依然受到保护 | |
| D. | 在铁制品上镀铜时,铁制品作电镀池的阳极,铜盐为电镀液 |
分析 A.锌、铁和海水构成原电池,锌为负极,被消耗,铁为正极,被保护;
B.原电池工作时负极失去电子,电流由正极经外电路流向负极,原电池中电解质溶液流向正极;
C.Zn比Fe活泼,破损后形成原电池中Zn为负极;
D.镀铜时,Cu为阳极,失去电子.
解答 解:A.作原电池负极的金属加速被腐蚀,作原电池正极的金属被保护,锌、铁和海水构成原电池,锌作负极,铁作正极被保护,该保护方法为牺牲阳极的阴极保护法,故A正确;
B.电流的方向与电子的运动方向相反,原电池工作时电流由正极经外电路流向负极,原电池中电流流向为电解质溶液到正极,故B正确;
C.Zn比Fe活泼,破损后形成原电池中Zn为负极,则铁皮依然受到保护,故C正确;
D.镀铜时,Cu为阳极,失去电子,而铁制品作电镀池的阴极,铜盐为电镀液,故D错误;
故选D.
点评 本题考查了原电池和电解池的原理,电极反应的分析,离子的移动是解题关键,题目较简单.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+ K+ SO42- HCO3- | B. | Cu2+ K+ SO42- NO3- | ||
| C. | Na+ K+Cl- NO3- | D. | Fe3+ K+ SO42- Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青石棉是一种硅酸盐材料 | |
| B. | 青石棉中含有一定量的石英晶体 | |
| C. | 青石棉的化学组成可表示为Na2O•3FeO•Fe2O3•8SiO2•H2O | |
| D. | 1mol青石棉能使1molHNO3被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | C(N2)/mol.L-1 | C(H2)/mol.L-1 | C(NH3)/mol.L-1 |
| 0 | 0.6 | 1.8 | 0 |
| 5 | 0.48 | X | 0.24 |
| 10 | 0.26 | 0.78 | 0.68 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
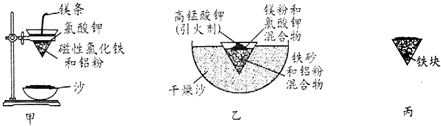
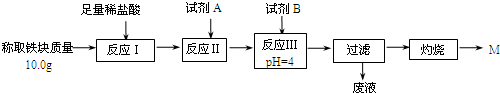
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在铜片上 Cu+2H+=Cu2++H2↑ | |
| B. | 氢氧化镁与盐酸的反应 H++OH-=H2O | |
| C. | 澄清石灰水与盐酸的反应 Ca(OH)2+2H+=Ca2++2H2O | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉投入氢氧化钠溶液中:2Al+2OH-═2AlO${\;}_{2}^{-}$+H2↑ | |
| B. | 硫酸与氢氧化钠溶液反应:H++OH-═H2O | |
| C. | 大理石与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| D. | 硫酸铜溶液和氢氧化钡溶液反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com