
 元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.
元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.分析 (1)同一主族元素,元素的非金属性越强,其氢化物的稳定性越强、其最高价氧化物的水化物酸性越强、其单质的氧化性越强,据此判断;
(2)工业上,通过如下转化可制得KClO3晶体:NaCl溶液$→_{Ⅰ}^{80℃通电}$NaClO3溶液$→_{Ⅱ}^{室温,HCl}$KClO3晶体,
①电解时,阳极上氯离子放电生成氯酸根离子、阴极上氢离子放电生成氢气;
②相同温度下,溶解度小的物质先析出;
(3)B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol.
解答 解:(1)a.Cl2、Br2、I2的熔点与分子间作用力有关,与非金属性无关,故a错误;
b.单质的氧化性越强,则非金属性越强,可以根据Cl2、Br2、I2的氧化性来判断非金属性,故b正确;
c.氢化物的稳定性越强,则非金属性越强,可以根据HCl、HBr、HI的热稳定性来判断非金属性,故c正确;
d.不能根据HCl、HBr、HI的酸性强弱来判断元素的非金属性,故d错误.
故答案为:bc;
(2)工业上,通过如下转化可制得KClO3晶体:NaCl溶液$→_{Ⅰ}^{80℃通电}$NaClO3溶液$→_{Ⅱ}^{室温,HCl}$KClO3晶体,
①电解时,阳极上氯离子放电生成氯酸根离子、阴极上氢离子放电生成氢气,所以反应方程式为1NaCl+3H2O═1NaClO3+3H2↑,
故答案为:1;3;1;3;H2↑;
②相同温度下,溶解度小的物质先析出,室温下KClO3在水中的溶解度明显小于其它晶体,所以先析出KClO3,
故答案为:室温下KClO3在水中的溶解度明显小于其它晶体;
(3)B→A+C,根据转移电子守恒得该反应方程式为3ClO-=ClO3-+2Cl-,反应热=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol,所以生成1molC时,放出117kJ热量;
故答案为:3ClO-=ClO3-+2Cl-;放出117.
点评 本题以卤族元素为载体考查了氧化还原反应、热化学反应、非金属强弱的判断方法等知识点,根据物质的性质、原子结构结合元素周期律等知识点来分析解答,题目难度中等.


科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4溶于水的部分能够电离,所以BaSO4是电解质 | |
| B. | SO2的水溶液能够导电,所以SO2是电解质 | |
| C. | 液态Cl2不导电,所以Cl2是非电解质 | |
| D. | 盐酸能导电,所以盐酸是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①③⑤ | C. | ②④⑧ | D. | ①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液 | B. | BaCl2溶液 | C. | NaOH溶液 | D. | 澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是沙子的主要成分,纯净的SiO2是光纤制品的基本原料 | |
| B. | 水晶的基本结构单元是[SiO4]四面体结构 | |
| C. | 将游离态的氮转变为氮的化合物就是氮的固定,合成氨是一种人工固氮方法 | |
| D. | 将等物质的量的氯气和二氧化硫同时通入品红溶液中,褪色比二氧化硫通入品红溶液快 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
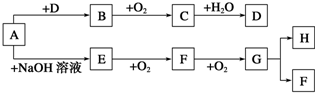
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 合成氨需用铁触媒加快反应速率 | |
| B. | 高压比常压有利于合成SO3的反应 | |
| C. | 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 | |
| D. | 收集氯气可用排饱和食盐水法 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com