
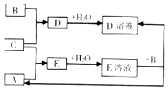
 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )
短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大.已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体.在适宜的条件下,A、B、C可以发生如图所示的反应.下列说法正确的是( )| A. | 化合物YX中含离子键 | B. | Z的含氧酸均为强酸 | ||
| C. | 非金属性:X>Z | D. | 离子半径:Y>Z |
分析 短周期元素X、Y、Z的原子序数依次增大,其中Y元素的原子半径最大,则Y为Na元素;已知A、B、C分别是X、Y、Z三种元素的单质,A和C常温下为气体,结合图中转化可知,B为Na,C为Cl2,D为NaCl,A为H2,E为HCl,盐酸与Na反应生成NaCl和氢气,均符合图中转化,即X为H,Y为Na,Z为Cl,以此来解答.
解答 解:由上述分析可知,X为H,Y为Na,Z为Cl,
A.NaH含离子键,故A正确;
B.若为HClO为弱酸,而Z的最高价含氧酸为强酸,故B错误;
C.非金属性Z>X,故C错误;
D.电子层越多,离子半径越大,则离子半径:Y<Z,故D错误;
故选A.
点评 本题考查无机物的推断,为高频考点,把握图中物质的转化、元素化合物知识为解答的关键,侧重分析与推断能力的考查,注意元素化合物及规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用新制的Cu(OH)2悬浊液检验淀粉是否水解完全 | |
| B. | 先滴加KSCN溶液无明显现象,再滴加H2O2溶液,检验溶液中是否含Fe2+ | |
| C. | 加热氯化铵固体制取适量氨气 | |
| D. | 用饱和碳酸氢钠溶液除去Cl2中含有的HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的乙烯和乙醇完全燃烧消耗氧气的量相等 | |
| B. | 戊烷和2-甲基丁烷是同系物 | |
| C. | 甲烷的二氯代物只有一种的事实,可证明甲烷为正四面体结构 | |
| D. | 三硝酸甘油酯的分子式为C3H5N3O9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实际应用 | 相应性质 | |
| A | 用含有酸性重铬酸钾溶液的仪器检验酒后驾车 | 乙醇具有还原性 |
| B | 明矾常用于自来水的净化、杀菌消毒 | 明矾可发生水解生成胶状的Al(OH)3 |
| C | BaSO4可作为造影剂检查肠胃道疾病 | BaSO4难溶于水且不与盐酸反应 |
| D | 过氧化钠可用作呼吸面具中的供氧剂 | Na2O2能与CO2反应生成O2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 验证Cl2的氧化性强于I2 | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液,可观察到溶液变成蓝色 |
| B | 配制100mL 1.0mol•L-1CuSO4溶液 | 将25gCuSO4•5H2O溶于100mL蒸馏水中 |
| C | 比较水与乙醇中氢的活泼性 | 分別将少量钠投入到盛有水和乙醇的烧杯中 |
| D | 验证Cu(OH)2的溶解度小于Mg(OH)2 | 将0.1mol•L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1CuSO4溶液,可观察到先有白色沉淀生成,后变为浅蓝色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
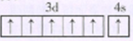 ;CrO2Cl2常温下为深红色液体,能与CCl4互溶,据此判断CrO2Cl2的晶体类型属于分子晶体.
;CrO2Cl2常温下为深红色液体,能与CCl4互溶,据此判断CrO2Cl2的晶体类型属于分子晶体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| B. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 氯苯分子中所有原子都处于同一平面 | |
| D. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | HY | C. | Y2 O | D. | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com