
| A. | c=$\frac{1000wρ}{M}$ | B. | m=$\frac{Vρw}{100}$ | C. | w=$\frac{cM}{1000ρ}$% | D. | c=$\frac{m}{VM}$ |
分析 体积为V mL,密度为ρ g/mL的含有相对分子质量为M的某物质的溶液,溶液的质量为Vρ,溶质的质量为mg,可根据c=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{1000ρw%}{M}$进行相关的计算与判断.
解答 解:A.物质的量浓度c=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{1000ρw%}{M}$mol/L,故A错误;
B.m=m(溶液)×w%=$\frac{Vρw}{100}$g,故B正确;
C.w%=$\frac{m(溶质的质量)}{m(溶液的质量)}$×100%=$\frac{V×1{0}^{-3}L×cmol/L×Mg/mol}{Vρg}$×100%=$\frac{cM}{1000ρ}$,故C错误;
D.c=$\frac{n}{V}$=$\frac{\frac{m}{M}mol}{V×1{0}^{-3}L}$=$\frac{1000m}{VM}$mol/L,故D错误;
故选B.
点评 本题考查物质的量浓度、溶质质量分数的计算,题目难度中等,试题侧重于物质的量的相关计算公式的综合运用,注意把握相关计算公式.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | 溴苯(溴) 加氢氧化钠再分液 | B. | 乙酸(乙醇)用蒸馏 | ||
| C. | 乙酸乙酯(乙酸)直接分液 | D. | 乙烷(乙烯)用酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
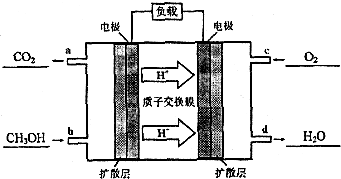 (1)在室温下测得0.1mol•L-1氨水PH=11,则该温度下氨水的电离度α=1.0%
(1)在室温下测得0.1mol•L-1氨水PH=11,则该温度下氨水的电离度α=1.0%查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉碘化钾溶液在空气中变蓝:4I+O2+2H2O═4OH-+2I2 | |
| B. | 用NaOH溶液吸收氯气:2OH-+2Cl2═2Cl-+H2O | |
| C. | 少量CO2通入苯酚钠溶液中:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| D. | 氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
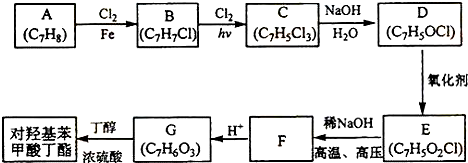
 ,该反应的类型为取代反应;
,该反应的类型为取代反应; ;
;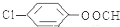 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述溶液能使甲基橙试剂变黄色 | |
| B. | 室温下,NH3•H2O是比HCN更弱的电解质 | |
| C. | 上述溶液中CN-的水解程度大于NH4+的水解程度 | |
| D. | 室温下,0.1mol/LNaCN溶液中,CN-的水解程度小于上述溶液中CN-的水解程度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com