
分析 (1)根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
(2)酸或酸式盐能电离出氢离子;
(3)电离出阴离子全是氢氧根离子的化合物为碱;根据物质的溶解性分析;
(4)根据物质的溶解性分析;
(5)在水溶液中和熔融状态下均不能导电的化合物,属于非电解质.
解答 解:①Cu是金属单质,能导电,既不是电解质也不是非电解质;
②NaCl是可溶性盐,溶于水和熔融状态下能导电;
③NaHSO4是酸式盐,能电离出氢离子,是电解质;
④CO2 不能导电,属于非电解质;
⑤H2SO4 溶于水能导电,能电离出氢离子,属于酸;
⑥酒精不能导电,属于非电解质;
⑦CaCO3 为难溶性盐,熔融状态下能导电,是电解质;
⑧BaSO4 为难溶性盐,熔融状态下能导电,是电解质;
⑨NaOH是碱,溶于水和熔融状态下均能导电,属于电解质,
故答案为:(1)②③⑤⑦⑧⑨;(2)③⑤;⑤;(3)⑨;(4)⑦⑧;(5)④⑥.
点评 本题考查学生酸碱盐概念及溶解性、电解质的判断,注意概念的整理和把握是关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 推广使用农药化肥,减少病虫害,提高粮食产量 | |
| B. | 开发新能源,减少化石能源的使用 | |
| C. | 开发新型电池,推广废旧电池的回收、处理经验 | |
| D. | 用“绿色化学”工艺,使原料完全转化为目标产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
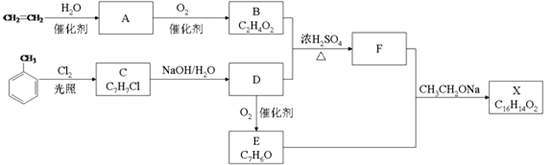
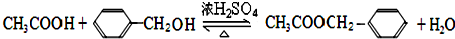 .
. .
.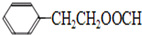 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、AlO2-、C1- | B. | ClO-、K+、OH一、HSO3- | ||
| C. | K+、Na+、SiO32-、SO42一 | D. | K+、A13+、Cl-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
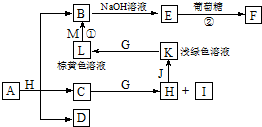 各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.
各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
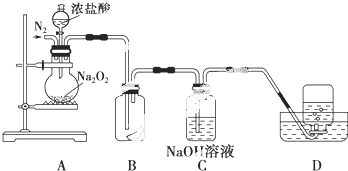
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com