
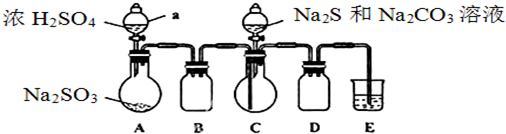
分析 (1)仪器a的名称是分液漏斗;E装置目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液、碳酸钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应;
(2)根据亚硫酸钡溶解于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸来分析;
(3)根据亚硫酸钠易被氧化生成硫酸钠分析;
(4)根据KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O反应方程式计算.
解答 解:(1)仪器a的名称是分液漏斗;E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液、碳酸钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应,故选bd,
故答案为:分液漏斗;bd;
(2)因为BaSO3难溶于水,可溶于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸,所以当沉淀未完全溶解,并有刺激性气味的气体产生,说明固体中既有硫酸钡又有亚硫酸钡,则可确定产品中含有Na2SO3和Na2SO4,
故答案为:若沉淀未完全溶解,并有刺激性气味的气体产生;
(3)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液,
故答案为:先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液;
(4)b中生成的碘在c中反应I2+2S2O32-═2I-+S4O62-,所以
I2 ~~~~~~2S2O32-,
1mol 2mol
1.0×10-5mol 2.0×10-3mol•L-1×0.010L=2.0×10-5mol,
根据KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O可知,KIO3的物质的量为$\frac{1}{3}$×10-5mol,所以精制盐的碘含量是$\frac{\frac{1}{3}×127×1{0}^{-5}×1{0}^{3}}{w×1{0}^{3}}$mg/kg=$\frac{1270}{w}$mg/kg,
故答案为:$\frac{1270}{w}$.
点评 题以某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3•5H2O)为载体,考查了物质的分离提纯、检验、设计优化等,综合性较强.


科目:高中化学 来源: 题型:选择题
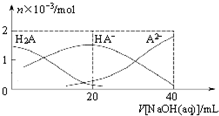 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )| A. | H2A属于强酸 | |
| B. | $\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大而减小 | |
| C. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol•L-1 | |
| D. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磷酸晶体和磷酸溶液 | B. | 硝酸钾晶体和熔化的硝酸钾 | ||
| C. | 蔗糖晶体和熔化的蔗糖 | D. | 熟石灰和澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  如果MnO2过量,浓盐酸就可全部消耗 | |
| B. |  量筒中发生了取代反应 | |
| C. |  生成蓝色的烟 | |
| D. |  干燥的有色布条褪色,说明氯气有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:K+、Na+、Cu2+、SO42- | |
| B. | c(OH-)=10-13 mol•L-1的溶液中:Al3+、NO3-、I-、Cl- | |
| C. | 水电离产生的c(H+)=10-13 mol•L-1的溶液中:Na+、Cl-、NO3-、SO42- | |
| D. | 0.1 mol•L-1FeSO4溶液中:K+、NH4+、MnO4-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H═-368.15 kJ•mol-1 | |
| B. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H═-736.3 kJ•mol-1 | |
| C. | CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H═-675.3 kJ•mol-1 | |
| D. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H═-1 472.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X溶液 | 物质Y |
| A | CuCl2 | 1mol Cu(OH)2 |
| B | KOH | 1mol KOH |
| C | Na2SO4 | 1mol H2SO4 |
| D | AgNO3 | 0.5mol Ag2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com