
| A. | ②④ | B. | ①③ | C. | ②③ | D. | ①④ |
分析 电离常数越大物质酸性越强,已知电离平衡常数:H2CO3>HClO>HCO3-,则酸性强弱顺序为:H2CO3>HClO>HCO3-,结合反应中强酸制备弱酸的规律解答.
解答 解:①H2CO3>HClO>HCO3-,则NaClO溶液中通入少量二氧化碳反应生成次氯酸和碳酸氢钠,故①错误;
②次氯酸酸性强于碳酸氢钠弱于碳酸,依据强酸制备弱酸规律,Na2CO3溶液中加入HClO溶液:CO32-+HClO═HCO3-+ClO-,故②正确;
③氯气与水反应生成氯化氢和次氯酸,氯化氢与碳酸钠反应生成氯化钠、碳酸氢钠和水,次氯酸与碳酸氢钠不反应,则离子方程式::Cl2+CO32-+H2O═HCO3-+Cl-+HClO,故③正确;
④Cl2通入NaHCO3溶液中,氯气与水反应生成盐酸和次氯酸,盐酸能够与碳酸氢钠反应生成氯化钠和水、二氧化碳,次氯酸酸性弱于碳酸,所以与碳酸氢钠不反应,应以次氯酸分子形式存在,故④错误;
故选:C.
点评 本题考查了离子方程式的书写正误判断,依据电离常数判断酸性强弱,明确强酸制备弱酸规律是解题关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
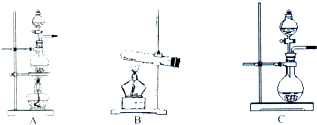 如表是实验室制备气体的有关内容:
如表是实验室制备气体的有关内容:| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | C |
| ② | 制氨气 | NH4Cl→NH3 | B |
| ③ | 制氯气 | HCl→Cl2 | A或C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在任何温度下都能自发进行 | B. | 在任何温度下都不能自发进行 | ||
| C. | 仅在高温下自发进行 | D. | 仅在低温下自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去KCl溶液中的少量K2CO3:加入适量的盐酸 | |
| B. | 除去CO2中的少量HCl:通入NaOH溶液 | |
| C. | 除去NaCl溶液中的少量MgCl2:加入适量KOH溶液,过滤 | |
| D. | 除去N2中的少量O2:通过灼热的CuO粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
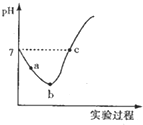 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol/L的NaOH溶液,整个实验过程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验过程中可用pH试纸测定溶液的pH | |
| B. | a点的溶液中:C(H+)=c(Cl-)+c(HCl0)+c(OH-) | |
| C. | c 点所示溶液中;c(Na+)=2c(ClO )+c(HCIO) | |
| D. | 由a点到b点的过程中,溶液中$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐可以作为调味剂,也可以调节体液电解质平衡 | |
| B. | 食品保鲜膜、塑料水杯等生活用品的主要成分是聚乙烯 | |
| C. | 化工生产中煤的干馏、石油的分馏、天然气生产甲醇均属于化学变化 | |
| D. | 高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验方案 | 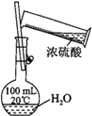 | 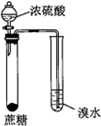 | 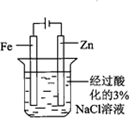 | 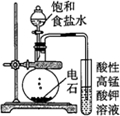 |
| 实验目的 | 配制一定物质的量浓度的硫酸 | 验证浓硫酸具有脱水性、氧化性 | 验证Fe电极被保护 | 用该装置制备并检验乙炔 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com