
 (1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为Pb2O3
(1)某小组分析二氧化铅分解产物的组成,取478g的PbO2加热,PbO2在加热过程发生分解的失重曲线如图所示,已知失重曲线上的a为96.66%,则a点固体的分子式为Pb2O3分析 (1)a点残余固体质量分数为96.66%,则残余固体质量为478g×99.66%,加热过程中Pb元素质量不变,则Pb元素物质的量为478g÷239g/mol=2mol,残留固体中O元素质量为478g×99.66%-2mol×207g/mol=48g,则O原子物质的量为48g÷16g/mol=3,Pb、O原子数目之比为2:3,故a点化学式为Pb2O3,相当于PbO2、PbO按物质的量1:1混合,由题目信息可知,Pb2O3与硝酸反应生成PbO2、Pb(NO3)2与水;
(2)①CH3COOH一CH3COONa溶液中PbO2与KI全部反应而溶解,得到棕色溶液,说明生成碘单质,PbO2被还原生成醋酸铅,还生醋酸钾与水;
②PbO2具有强氧化性,可以将盐酸中氯离子氧化为氯气,同时生成PbCl2与水;酸性条件下Na2S2O3会反应得到S、SO2;
③分离互不相溶的固体与液体,应采取过滤方法,并需要洗涤、干燥,所得固体相当于PbO2、PbO的混合物,根据PbO2~I2~2Na2S2O3计算PbO2的物质的量,再根据PbO~Pb(NO3)2~PbCrO2计算PbO的物质的量,进而确定固体化学式.
解答 解:(1)a点残余固体质量分数为96.66%,则残余固体质量为478g×99.66%,加热过程中Pb元素质量不变,则Pb元素物质的量为478g÷239g/mol=2mol,残留固体中O元素质量为478g×99.66%-2mol×207g/mol=48g,则O原子物质的量为48g÷16g/mol=3,Pb、O原子数目之比为2:3,故a点化学式为Pb2O3,相当于PbO2、PbO按物质的量1:1混合,由题目信息可知,Pb2O3与硝酸反应生成PbO2、Pb(NO3)2与水,反应方程式为:Pb2O3+2HNO3=PbO2+Pb(NO3)2+H2O,
故答案为:Pb2O3;Pb2O3+2HNO3=PbO2+Pb(NO3)2+H2O;
(2)①CH3COOH一CH3COONa溶液中PbO2与KI全部反应而溶解,得到棕色溶液,说明生成碘单质,PbO2被还原生成醋酸铅,还生醋酸钾与水,反应方程式为:PbO2+2KI+4CH3COOH=(CH3COO)2Pb+2CH3COOK+I2+2H2O,
故答案为:PbO2+2KI+4CH3COOH=(CH3COO)2Pb+2CH3COOK+I2+2H2O;
②PbO2具有强氧化性,可以将盐酸中氯离子氧化为氯气,同时生成PbCl2与水,反应方程式为:PbO2+4HCl=PbCl2+Cl2↑+H2O,
酸性条件下Na2S2O3会反应得到S、SO2,反应方程式为:Na2S2O3+2CH3COOH=2CH3COONa+S↓+SO2↑+H2O,
故答案为:PbO2+4HCl=PbCl2+Cl2↑+H2O;Na2S2O3+2CH3COOH=2CH3COONa+S↓+SO2↑+H2O;
③采取过滤方法分离出固体,再洗涤、干燥,所得固体相当于PbO2、PbO的混合物,
根据PbO2~I2~2Na2S2O3,可知n(PbO2)=$\frac{1}{2}$n(Na2S2O3)=$\frac{1}{2}$×0.02L×0.2mol/L=0.002mol,根据PbO~Pb(NO3)2~PbCrO2,可知n(PbO)=n(PbCrO2)=$\frac{0.969g}{323g/mol}$=0.003mol,故PbO2、PbO的物质的量之比为0.002mol:0.003mol=2:3,则固体化学式为Pb5O7,
故答案为:过滤、洗涤、干燥;Pb5O7.
点评 本题考查化学方程式计算、物质组成测定等,是对学生综合能力的考查,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蓝色石蕊试纸褪色 | B. | 蓝色石蕊试纸变红 | ||
| C. | 蓝色石蕊试纸先变红再褪色 | D. | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 、
、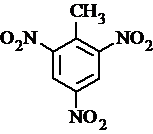 等
等 .
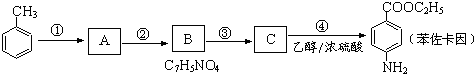
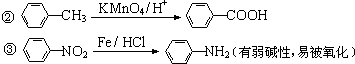
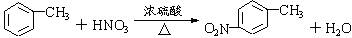
.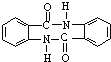 有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图.提示:①合成过程中无机试剂任选;②合成路线流程图示例如下:
有较好的阻燃性,请写出以甲苯为主要原料制备该阻燃剂的合成路线流程图.提示:①合成过程中无机试剂任选;②合成路线流程图示例如下: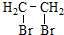
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上常以海带或其它海产品为原料提取碘 | |
| B. | 炼铁和制玻璃的工业中都要用到石灰石 | |
| C. | 氯气通入石灰乳中制漂白粉 | |
| D. | 电解氯化钠溶液制金属钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com