
下列有关化学反应速率与限度的说法,正确的是
A.任何可逆反应都有一定的限度,且限度是可以改变的
B.对任何化学反应来说,反应速率越大,则现象越明显
C.决定化学反应速率的主要因素是温度、浓度、压强
D.铁与稀硫酸反应制氢气时,改用98.3%的浓疏酸,对增大化学反应速率明显有效
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:2017届重庆八中高三上学期定时训练14化学试卷(解析版) 题型:填空题
化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH-=FeO42-+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42-,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只有在强碱性条件下稳定,易被H2还原。
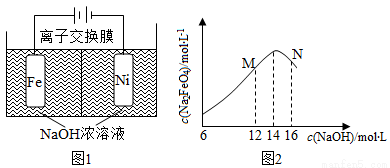
①电解一段时间后,c(OH-)降低的区域在__________(城 “阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是________。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
根据表中信息判断,下列选项正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2 、H2SO4 | K2SO4 、MnSO4 .. |
② | Cl2 、FeBr2 | FeCl3 、Br2 |
③ | MnO2...... | Cl2 、Mn2+ ... |
A.第①组反应的其余产物为H2O
B.第③组反应中生成1mol Cl2,转移电子4mol
C.氧化性由强到弱顺序为MnO4- > Fe3+>Cl2 >Br2
D.第②组反应中Cl2 与 FeBr2的物质的量之比为3:2
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
在温度相同时,100mL0.01mol/L的CH3OOH溶液与10mL0.1mol/LCH3COOH溶液相比较,下列叙述中前者大于后者的是( )
A.CH3OOH的物质的量
B.溶液中的n(H+)
C.用同浓度的NaOH溶液恰好完全反砬,消耗NaOH溶液的体积
D.溶液的导电能力
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
下列说法正确的是
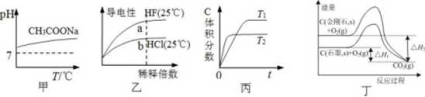
A.由图甲可知,升高温度醋酸钠的水解程度增大
B.由图乙可知,a点Kw的数值比b点Kw的数值大
C.由图丙可知,反应A(g)+B(g) 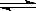 2C(g)是吸热反位
2C(g)是吸热反位
D.由图丁可知,反应C(金刚石,s)=C(石墨,s)的焓变△H=△H1-△H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:推断题
下图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)

请回答下列问题:
(1)物质A的化学式为__________。组成单质C的原子结构示意图__________。
(2)反应①的化学方程式为__________;反应②的化学方程式为__________。
(3)设计实验验证一包纯净物是H_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:选择题
实验室提纯含少量氯化钠杂质的硝酸钾的过程如下图所示。下列分析正确的是
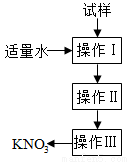
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩。趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D. 操作Ⅰ~Ⅲ总共需两次过滤
操作Ⅰ~Ⅲ总共需两次过滤
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:选择题
研究化学反应常用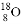 作为示踪原子,该原子的质子数是
作为示踪原子,该原子的质子数是
A. 18 B. 8 C. 10 D. 16
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安中学高二实验班上期中化学卷(解析版) 题型:选择题
用某种仪器量取液体体积,平视时读数为 n mL,仰视时读数为 x mL,俯视时读数为 y mL,若 x>n>y,则所用的仪器可能为
A. 量筒 B. 容量瓶 C. 滴定管 D. 以上均不对
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com