
| A. | 要证明硫酸亚铁铵晶体中含有NH4+,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体 | |
| B. | KClO3、KNO3、KMnO4等强氧化剂或其混合物不能研磨,否则将引起爆炸 | |
| C. | 常温下用pH试纸分别测定0.1mol•L-1NaClO溶液和0.01mol•L-1NaClO溶液的pH,可以比较浓度对水解程度的影响 | |
| D. | 过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 |
分析 A.检验氨气选用红色的石蕊试纸;
B.强氧化剂研磨易发生分解反应;
C.NaClO溶液具有漂白性;
D.萃取、分液和蒸馏等都是常用的分离有机混合物的方法.
解答 解:A.要证明硫酸亚铁铵晶体中含有NH4+,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,生成氨气,再用湿润的红色石蕊试纸检验产生的气体,故A错误;
B.强氧化剂研磨易发生分解反应,生成气体导致爆炸,则KClO3、KNO3、KMnO4等强氧化剂或其混合物不能研磨,否则将引起爆炸,故B正确;
C.NaClO溶液具有漂白性,不能使用pH试纸测定其pH,可选pH计,故C错误;
D.萃取、分液和蒸馏等都是常用的分离有机混合物的方法,而过滤、结晶主要应用无机混合物的分离,故D错误;
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、混合物分离提纯方法等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
 转变成
转变成 的方法是( )
的方法是( )| A. | 加入足量的NaOH(aq)并加热 | |
| B. | 与盐酸共热后,再加入足量的NaOH溶液 | |
| C. | 与足量NaOH溶液共热后,再通入足量CO2 | |
| D. | 与稀硫酸共热后,加入足量Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 三氯化铁溶液跟氨水反应:Fe3++3NH3•H2O═Fe(OH)3↓+3NH4+ | |
| C. | 碳酸氢钙溶液跟稀硝酸反应:Ca(HCO3)2+2H+═Ca2++2H2O+2CO2↑ | |
| D. | 常温下将氯气通入氢氧化钠溶液:2Cl2+2OH-═3Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “双吸剂”中的无机盐和生石灰都有吸水作用 | |
| B. | “双吸剂”吸收水时,发生了原电池反应 | |
| C. | 吸收氧气的过程中,铁粉作原电池的正极 | |
| D. | 炭粉上发生的反应为:O2+4e-+2H2O=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 | |
| B. | ab段发生的离子反应为:Al3++3OH-=Al(OH)3↓,Mg2++2OH-=Mg(OH)2↓ | |
| C. | 原溶液中含有的阳离子必定有H+、NH4+、Al3+、Mg2+ | |
| D. | d点溶液中含有的溶质只有Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅可以用于制造变压器的铁芯材料 | |
| B. | 硫可用于制造黑火药 | |
| C. | 二氧化硅可用于制造光导纤维 | |
| D. | 氢氧化铝既能吸附水中悬浮物,又能吸附色素,故可用于净水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2,4二甲基-3-乙基己烷
2,4二甲基-3-乙基己烷查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
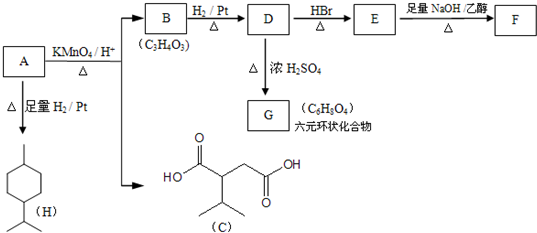
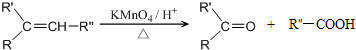
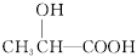 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$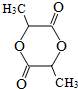 +2H2O.
+2H2O.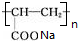 .
.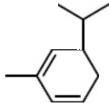 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com