
| A. | 25%和7.5akJ | B. | 25%和3bkJ | C. | 75%和(a-b) kJ | D. | 75%和(10a-b) kJ |
分析 从氨气开始进行化学反应,平衡时各组分的含量相同,二者为等效平衡:
若为恒温恒容,按化学计量数转化到左边满足n(N2)=10mol、n(H2)=30mol即可,根据原平衡时氢气转化率计算原平衡体系中氢气的物质的量,据此计算参加反应的氨气的物质的量,再根据转化率定义计算,根据反应中能量守恒计算吸收的热量;
若为恒温恒压,按化学计量数转化到左边满足n(N2):n(H2)=10mol:30mol=1:3即可,n(N2):n(H2)=1:3等于化学计量数之比,故氨气的物质的量为任意值,氨气的转化率与恒温恒容条件下相同,根据反应中能量守恒计算吸收的热量.
解答 解:从氨气开始进行化学反应,平衡时各组分的含量相同,二者为等效平衡:
若为恒温恒容,按化学计量数转化到左边满足n(N2)=10mol、n(H2)=30mol,氮气与氢气的物质的量之比等于化学计量数之比,由方程式可知n(NH3)=2n(N2)=2×10mol=20mol,
原平衡时氮气转化率为25%,则原平衡体系中氮气的物质的量为10mol×(1-25%)=7.5mol,故从氨气建立平衡生成的氮气为7.5mol,由方程式可知,参加反应的氨气的物质的量为7.5mol×2=14mol,故从氨气建立等效平衡,氨气的转化率为:$\frac{15mol}{2mol}$×100%=70%;
若为恒温恒压,按化学计量数转化到左边满足n(N2):n(H2)=10mol:30mol=1:3即可,n(N2):n(H2)=1:3等于化学计量数之比,故氨气的物质的量为任意值,氨气的转化率为75%,
根据反应中能量守恒可知,正逆反应中反应热的数值相等,符号相反,所以反从氨气开始时,达到与原平衡为等效平衡,则吸收的热量为(a-b) kJ,
故选C.
点评 本题考查等效平衡的有关计算,难度中等,注意理解等效平衡规律,本题的易错点为可逆反应中反应热的应用.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:填空题

| V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
| E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
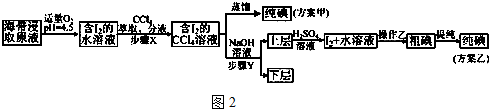
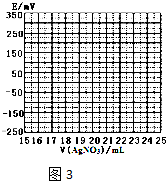
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 1 mol/L的NaCl溶液 | B. | 75mL 2 mol/L的NH4Cl溶液 | ||
| C. | 150mL 3 mol/L的KCl溶液 | D. | 75mL 1 mol/L的BaCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | ||||||||
| 二 | A | B | C | |||||
| 三 | D | E | F | G |
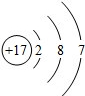 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 35℃ |
| K | 2.041 | 0.270 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1molCO 2molH2 | 2mol CH3OH | 2mol CH3OH | |
| 平 均 数 据 | CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | aKJ | bKJ | cKJ | |
| 体系压强 | P1 | P2 | P3 | |
| 反转化率应物 | a1 | a2 | a3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
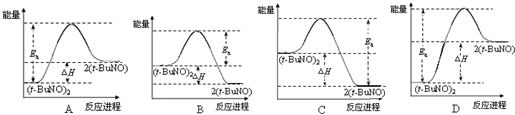
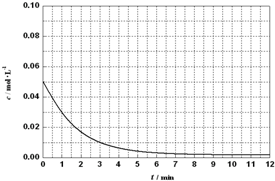
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30g丙醇中存在的共价键总数为5NA | |
| B. | 密闭容器中2mol NO与1mol O2充分反应,转移的电子数为2NA | |
| C. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子总数为2NA | |
| D. | 2.8g乙烯和环丁烷(C4H8)的混合气体中含有的原子总数为0.6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com