
| 食物 | 苹果 | 葡萄 | 玉米 | 牛奶 |
| pH | 2.9~3.3 | 3.5~4.5 | 6.8~8.0 | 6.3~6.6 |
| A. | 玉米 | B. | 苹果 | C. | 葡萄 | D. | 牛奶 |
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:r(Z)>r(W)>r(Y) | |
| B. | Y的简单气态氢化物的热稳定性比W的强 | |
| C. | Z和Y形成的原子个数比为1:1和2:1的化合物中化学键类型相同 | |
| D. | X的最高价氧化物对应水化物的酸性比W的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
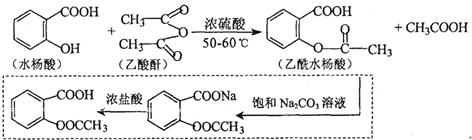
 .
. .
.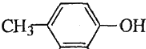 也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件:
也能与乙酸酐发生类似反应,请写出化学反应方程式,可不写条件: .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用PH试纸可测得某溶液的pH为6.5 | |
| B. | 可用25mL碱式滴定管量取20.00mLKMnO4溶液 | |
| C. | 石油、煤、天然气、可燃冰、植物油都属于化石燃料 | |
| D. | 把CO中毒的病人放入高压氧仓中解毒,其原理符合勒夏特列原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 名称 | 分子式 | 结构式 | 结构简式 |
| 乙烯 | C2H4 |  | \ |
| 丙烯 | C3H6 | \ | CH3-CH=CH2 |
| 乙炔 | \ | H-C≡C-H | |
| 异丁烷 | \ | CH3CH(CH3)CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com