
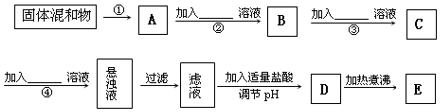
分析 将混有K2SO4、MgSO4的KNO3固体溶解,配制成溶液,先加氢氧化钾溶液,除去镁离子,生成C含有氢氧化镁沉淀,再加硝酸钡溶液,除去硫酸根,生成硫酸钡沉淀,再加碳酸钾,除去多余的钡离子,过滤除去沉淀得到滤液,在滤液中加入硝酸,除去多余的碳酸钾和氢氧化钾,硝酸易挥发,加热煮沸,制得纯净的KNO3溶液(E),加入盐酸调节溶液的pH会引进Cl-,以此解答该题.
解答 解:(1)固体应先溶解,由题给信息可知加入KOH,可得到Mg(OH)2沉淀,故答案为:溶解;Mg(OH)2;
(2)由分析可知,操作③所加的试剂为Ba(NO3)2,反应的离子方程式为 Ba2++SO42-═BaSO4↓,故答案为:Ba(NO3)2; Ba2++SO42-═BaSO4↓;
(3)操作④所加的试剂为K2 CO3,用于除去钡离子,方程式为Ba2++CO32-═BaCO3↓,故答案为:K2 CO3; Ba2++CO32-═BaCO3↓;
(4)加入盐酸调节溶液的pH会引进Cl-,应加入硝酸酸化,故答案为:否;调节PH值时改用适量硝酸.
点评 本题综合考查物质的分离、提纯以及制备,为高频考点,侧重于学生的分析和实验能力的考查,注意把握物质的性质的异同,考虑实验设计的严密性,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
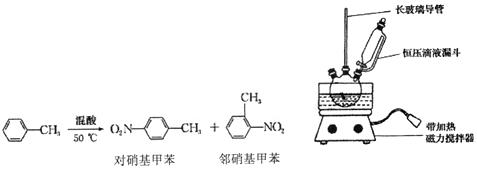
| 密度/(g•cm-3) | 沸点/℃ | 式量 | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 92 | 不溶于水,易溶于一硝基甲苯 |
| 对硝基甲苯 | 1.286 | 237.7 | 137 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 137 | 不溶于水,易溶于液态烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 乙同学正确 | 选用试剂 | 实验现象 |
| 第一种方法 | ||
| 第二种方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
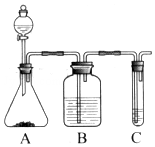 实验室常用如图中的装置制备乙炔并检验乙炔的性质:
实验室常用如图中的装置制备乙炔并检验乙炔的性质:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
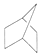 C.CH2=CH-CH=CH2 D.HOOCCH2CH2CH2Cl
C.CH2=CH-CH=CH2 D.HOOCCH2CH2CH2Cl
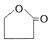 则E的结构简式NaOOCCH2CH2CH2OH,F生成五元环酯的化学方程式HOOCCH2CH2CH2OH$→_{△}^{浓硫酸}$
则E的结构简式NaOOCCH2CH2CH2OH,F生成五元环酯的化学方程式HOOCCH2CH2CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2Mn5O10是氧化产物 | |
| B. | 正极反应式:Ag-e-═Ag+ | |
| C. | Cl-不断向“水”电池的正极移动 | |
| D. | 毎转移2mol电子,负极质量增加71克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
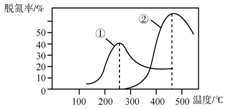 工业上采用NH3作还原剂脱氮原理为:NO(g)+NO2(g)+2NH3(g)?2N2(g)+3HO(g),烟气以一定的流速通过,测量不同温度下逸出气体中氮氧化物含量,从而确定烟气效率,右图是两种不同催化剂的脱氮效率曲线,判断以下分析不正确的是( )
工业上采用NH3作还原剂脱氮原理为:NO(g)+NO2(g)+2NH3(g)?2N2(g)+3HO(g),烟气以一定的流速通过,测量不同温度下逸出气体中氮氧化物含量,从而确定烟气效率,右图是两种不同催化剂的脱氮效率曲线,判断以下分析不正确的是( )| A. | 上述反应的正反应为放热反应 | |
| B. | 催化剂①、②分别适合于250℃和450℃左右脱氮 | |
| C. | 曲线①、②最高点表示此时平衡转化率最高 | |
| D. | 相同条件下,改变压强对脱氮率没有影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com