
【题目】化学反应的实质是( )
A.能量的转移
B.旧化学键断裂和新化学键生成
C.电子转移
D.原子种类与原子数目保持不变
科目:高中化学 来源: 题型:
【题目】如图1,天宫二号空间实验室已于2016 年9月15日22时04分在酒泉卫星发射中心发射成功.请回答下列问题:
(1)耐辐照石英玻璃是航天器姿态控制系统的核心元件.石英玻璃的成分是(填化学式),该物质的类别属于(填“碱性氧化物”或“酸性氧化物”),实验室中不能用玻璃塞试剂瓶盛放KOH溶液,原因是(用离子方程式表示)
(2)“碳纤维复合材料制品”应用于“天宫二号”的推进系统.碳纤维复合材料具有重量轻、可设计强度高的特点.碳纤维复合材料由碳纤维和合成树脂组成,其中合成树脂是高分子化合物,则制备合成树脂的反应类型是 .
(3)太阳能电池帆板是“天宫二号”空间运行的动力源泉,其性能直接影响到“天宫二号”的运行寿命和可靠性.
①天宫二号使用的光伏太阳能电池,该电池的核心材料是 , 其能量转化方式为 .
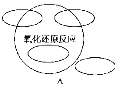
②如图2是一种全天候太阳能电池的工作原理:太阳照射时的总反应为V3++VO2++H2O=V2++VO2++2H+ , 则负极反应式为;夜间时,电池正极为(填“a”或“b”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.0500molL﹣1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000molL﹣1NaOH溶液所得滴定曲线如图.下列说法正确的是( ) 
A.点①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O4﹣)=c(OH﹣)
B.点②所示溶液中:c(HC2O4﹣)+2c(C2O42﹣)=c(Na+)
C.点③所示溶液中:c(Na+)>c(HC2O4﹣)>c(H2C2O4)>c(C2O42﹣)
D.滴定过程中可能出现:c(Na+)>c(C2O42﹣)=c(HC2O4﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明BF3为平面三角形而不是三角锥形分子的理由是( )
A.BF2Cl只有一种结构B.三根B﹣F键间键角都为120°
C.BFCl2只有一种结构D.三根B﹣F键键长都为130pm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)A图是“四种基本反应类型与氧化还原反应的关系”图,请在A图中用阴影部分表示反应:H2+CuO![]() Cu+H2O所属的区域。
Cu+H2O所属的区域。
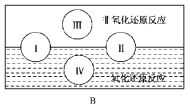
(2)“四种基本反应类型与氧化还原反应的关系”也可用B图表达。其中Ⅰ为化合反应,则Ⅱ为________反应。写出有水生成的符合反应类型Ⅲ的一个化学方程式:____________________。写出有水参加的符合反应类型Ⅳ的一个化学方程式_____________,其中水________(填“被氧化”或“被还原”或“既被氧化又被还原”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4![]() 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________。
(2)As2O3在上述反应中显示出来的性质是____________(填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中水只表现还原性的是
A. 3NO2+H2O=2HNO3+NO
B. 2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
C. 2F2+2H2O=4HF+O2
D. 2Na+2H2O=2NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是( ) 
A.a电极上发生的反应为:MnO4﹣+8H++5e﹣═Mn2++4H2O
B.外电路电子的流向是从a到b
C.电池工作时,盐桥中的SO42﹣移向甲烧杯
D.b电极上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《华北电力大学学报:社会科学版》2014年第2期的文章《欧盟暂停征收航空碳排放税的法律思考》,该文章从欧盟暂停征收航空碳排放税的背景人手,分析了欧盟征收航空碳排放税的争议焦点所在,最后对欧盟暂停征收航空碳排放税进行了评析,并提出征收航空碳排放税是未来趋势的观点,希望在反对声中换一个视角来阐述征收航空碳排放税对于环境保护、技术革新和国际法的促进作用.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
C+KMnO4+H2SO4=CO2↑+MnSO4+K2SO4+H2O
(2)在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
n/mol | 活性炭 | NO | E | F |
初始 | 2.030 | 0.100 | 0 | 0 |
T1 | 2.000 | 0.040 | 0.030 | 0.030 |
T2 | 2.005 | 0.050 | 0.025 | 0.025 |
上述反应T1℃时的平衡常数为K1 , T2℃时的平衡常数为K2 .
①计算:K1=
②根据上述信息判断,温度T1和T2的关系是(填序号) .
A. T1>T2 B. T1<T2 C.无法比较
(3)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)CO2(g)+H2(g);△H=﹣41kJ/mol
已知:2H2O (g)═2H2(g)+O2(g);△H=+484kJ/mol,
①写出CO完全燃烧生成CO2的热化学方程式: .
②某温度下,在一容积可变的容器中,CO转化生成CO2的反应达到平衡时,CO、O2和CO2的物质的量分别为4mol、2mol、和4mol.保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是:(填序号) .
A. 均增加1mol B. 均加倍 C. 均减少1mol D. 均减半.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com