
| A. | 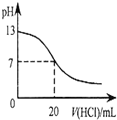 表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 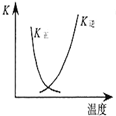 图中曲线表示反应2SO2(g)+O2(g)═2SO3(g)△H<0 正、逆反应的平衡常数K随温度的变化 | |
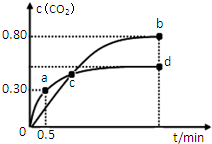
| C. | 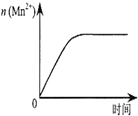 表示10 mL 0.01 mol•L-1 KMnO4酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. |  图中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
分析 A.当溶液pH=7时,氢氧化钠就与氯化氢恰好反应,滴定曲线应该有一个滴定突变;
B.该反应为放热反应,温度升高,平衡向着逆向移动,K(逆)增大、K(正)减小;
C.n(Mn2+)开始为0,随反应的发生,增大,氧化还原反应结束后,其物质的量不再变化;
D.催化剂降低反应所需的活化能.
解答 解:A.用盐酸滴定氢氧化钠溶液,当恰好中和时溶液的pH=7,酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,题中图象变化与实际不相符,故A错误;
B.因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K(逆)会增大,而K(正)会减小,图象中变化与实际上的变化相符,故B正确;
C.n(Mn2+)开始为0,随反应的发生,增大,氧化还原反应结束后,其物质的量不再变化,与图象一致,故C正确;
D.催化剂降低反应所需的活化能,反应的始态、终态相同,曲线a为使用催化剂的情况,与图象一致,故D正确;
故选A.
点评 本题考查了图象与中和滴定、化学平衡等知识,题目难度中等,注意抓住图象的“形变神不变”对图象进行分析,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.


 特高级教师点拨系列答案
特高级教师点拨系列答案 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
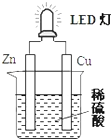
| A. | 铜片表面有气泡生成,锌片上发生氧化反应 | |
| B. | 如果将稀硫酸换成葡萄糖溶液,不能使LED灯发光 | |
| C. | 装置中存在“化学能→电能→光能”的转换 | |
| D. | 如果将铜片换成铁片,则锌片为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池放电时的负极和充电时的阳极均发生还原反应 | |
| B. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大 | |
| D. | 纯碱溶于热水中去污效果增强,说明纯碱的水解是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s);△H 1
利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s)?5CO2(g)+I2(s);△H 1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3既不是氧化剂也不是还原剂 | B. | 氧化剂与还原剂物质的量比是1:3 | ||
| C. | AlN是还原产物 | D. | 每生成1 mol AlN有2mol电子转移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com