
| A�� | ����ʱ����ˮ�����c��H+��=1.0��10-12mol•L-1����Һ�У�K+��Na+��HCO3-��Cl-һ���ܴ������� | |
| B�� | �����£���pH=4�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ����� | |
| C�� | �����£�pH=2�Ĵ�����Һ�������е�H+��Ϊ0.01 NA | |
| D�� | ��92 g N2O4������������У��ָ������³�ѹʱ�������������������NA |
���� A����ˮ�����c��H+��=1.0��10-12mol•L-1����Һ��Ϊ������Һ��
B�������£���pH=4�Ĵ�����Һϡ�ͺ�������Ũ�ȼ�С��Kw���䣻
C����Һ���δ֪��������n=cV���㣻
D������N2O4?2NO2��92 g N2O4��������ʵ���Ϊ1mol����Ӧ��ϵ����������ʵ�������1mol��
��� �⣺A����ˮ�����c��H+��=1.0��10-12mol•L-1����Һ��Ϊ������Һ��HCO3-���ᡢ�����Ӧ��һ�����ܹ��棬��A����
B�������£���pH=4�Ĵ�����Һϡ�ͺ�������Ũ�ȼ�С��Kw���䣬������������Ũ������B����
C����Һ���δ֪��������n=cV���㣬���ܼ���H+������C����
D������N2O4?2NO2��92 g N2O4��������ʵ���Ϊ1mol����Ӧ��ϵ����������ʵ�������1mol�������������������NA����D��ȷ��
��ѡD��
���� ���⿼����ۺϣ��漰���ӵĹ��桢pH�ļ��㡢������ʵĵ���ƽ�⼰��ѧƽ��ȣ�Ϊ��Ƶ���㣬���ճ�������֮��ķ�Ӧ����Ӧԭ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬�ۺ��Խ�ǿ����Ŀ�ѶȲ���


 �������¿��ÿ�ʱ��ҵϵ�д�
�������¿��ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
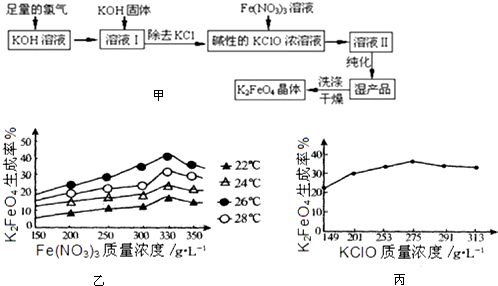
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A��C��D��B | B�� | A��B��C��D | C�� | C��A��D��B | D�� | C��B��D��A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��1 | B�� | 1��3 | C�� | 2��3 | D�� | 3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
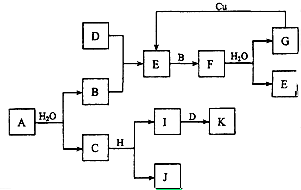 A��KΪ��ѧ��ѧ�ij������ʣ�����֮��������ͼ��ʾ��ת����ϵ����Ӧ��������ȥ������֪��ͨ��״���£�A�ǵ���ɫ���壬B��D��I������ɫ���嵥�ʣ�F�Ǻ���ɫ���壬H�ǽ������ʣ��ش��������⣺
A��KΪ��ѧ��ѧ�ij������ʣ�����֮��������ͼ��ʾ��ת����ϵ����Ӧ��������ȥ������֪��ͨ��״���£�A�ǵ���ɫ���壬B��D��I������ɫ���嵥�ʣ�F�Ǻ���ɫ���壬H�ǽ������ʣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
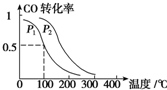 ��1��CO�Ǹ�¯��������Ҫ��Ӧ��֮һ����������Ҫ��ӦΪ��
��1��CO�Ǹ�¯��������Ҫ��Ӧ��֮һ����������Ҫ��ӦΪ��| �¶�/�� | 1 000 | 1 150 | 1 300 |
| ƽ�ⳣ�� | 4.0 | 3.7 | 3.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
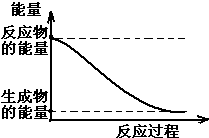 ��1��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ�Ƿ��ȣ�������ȡ����ȡ�����Ӧ��NO2��CO�����������ڣ���
��1��20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ��˵�������Ӧ�Ƿ��ȣ�������ȡ����ȡ�����Ӧ��NO2��CO�����������ڣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NO${\;}_{3}^{-}$ | B�� | -Cl | C�� | 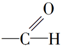 | D�� | -NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | [Ne]3s1[Ne]3s2 | B�� | [Ar]4s1[Ne]3s23p4 | ||
| C�� | [Ne]3s2[Ar]4s2 | D�� | [He]2s22p4[Ne]3s23p5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com