
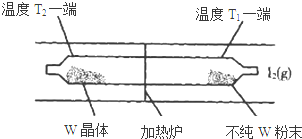
 利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0.
利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0.分析 (1)平衡常数指一定条件下,可逆反应达到平衡时,生成物浓度化学计量数次数幂之积与反应物浓度化学计量数次数幂之积的比值,注意固体、纯液体不需要写出;
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变,以此进行判断,注意选择的物理量随反应进行发生变化,该物理量由变化到不变化说明到达平衡;
(3)设反应的碘单质物质的量为x
W(s)+I2(g)?WI2(g)
起始量(mol) 1 0
变化量(mol) x x
平衡量(mol) 1-x x
K=$\frac{x}{1-x}$=$\frac{1}{3}$
x=0.25mol
则0-5min内的平均反应速率v(WI2)=$\frac{△c}{△t}$,转化率=$\frac{消耗量}{起始量}$×100%;
反应前后气体物质的量不变,加入碘单质物质的量为原来的2倍,I2的物质的量浓度为原来的2倍,平衡常数随温度变化,浓度增大达到平衡的时间短,最后达到的平衡相同;
(4)为提高该反应的反应速率,同时使$\frac{c({I}_{2})}{c(W{I}_{2})}$增大,说明平衡逆向进行,反应是放热反应,升温增大反应速率,平衡逆向进行;
(5)由图可知,在高温条件下得到纯的W晶体,即升高温度平衡向逆反应方向移动;反应体系中I2可循环使用.
解答 解:(1)①可逆反应W(s)+I2(g)?WI2(g)的平衡常数k=$\frac{[W{I}_{2}]}{[{I}_{2}]}$,故答案为:$\frac{[W{I}_{2}]}{[{I}_{2}]}$;
(2)a.平衡时I2与WI2浓度关系与转化率有关,二者浓度不一定相等,故a错误;
b.随反应进行,W质量分数变化,若W的质量不再变化,说明到达平衡,故b正确;
c.随反应进行,混合气体的质量发生变化,恒容条件下密度也在不断变化,若容器内混合气体的密度保持不变,说明反应达到平衡,故c正确;
d.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等,反应过程中压强始终不变,不能说明达到平衡,故d错误,
故答案为:bc;
(3)设反应的碘单质物质的量为x
W(s)+I2(g)?WI2(g)
起始量(mol) 1 0
变化量(mol) x x
平衡量(mol) 1-x x
K=$\frac{x}{1-x}$=$\frac{1}{3}$
x=0.25mol
则0-5min内的平均反应速率v(WI2)=$\frac{△c}{△t}$=$\frac{\frac{0.25mol}{2L}}{5min}$=0.025mol/(L•min),
平衡时I2(g)的转化率=$\frac{消耗量}{起始量}$×100%=$\frac{0.25mol}{1mol}$×100%=25%;
反应前后气体物质的量不变,加入碘单质物质的量为原来的2倍,I2的物质的量浓度为原来的2倍,平衡常数随温度变化,浓度增大达到平衡的时间短,最后达到的平衡相同,故选c;
故答案为:0.025mol/(L•min);25%;c;
(4)为提高该反应的反应速率,同时使$\frac{c({I}_{2})}{c(W{I}_{2})}$增大,说明平衡逆向进行,反应是放热反应,升温增大反应速率,平衡逆向进行,故答案为:升高温度;
(5)由图可知,在高温条件下得到纯的W晶体,即升高温度平衡向逆反应方向移动,正反应为放热反应,即△H<0,通过题意温度T2端利于反应正向进行,为低温,温度T1端利于反应向左进行,为高温,所以T1>T2;反应体系中I2可循环使用,
故答案为:>;I2.
点评 本题考查化学平衡常数、化学平衡计算、弱电解质的电离平衡常数、溶液离子浓度大小比较,侧重考查学生对知识迁移运用能力,注意比较溶液中各种离子浓度相对大小时要结合电荷守恒和物料守恒等分析解答,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 40 | B. | 65 | C. | 90 | D. | 120 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-48.40kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2 (g)+9H2O(l)△H=-5517.60kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-5517.60kJ•mol-1 | |
| D. | 2C8H18(l)+25O2(g)═16CO2 (g)+18H2O(l)△H=-11035.20kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
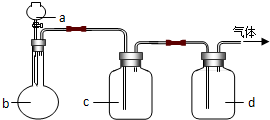 拟用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c.d表示相应仪器中加入的试剂).下列可以得到干燥纯净的气体的选项是( )
拟用如图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c.d表示相应仪器中加入的试剂).下列可以得到干燥纯净的气体的选项是( )| 选项 | 气体 | a | b | c | d |
| A | CO2 | 盐酸 | CaCO3 | 饱和Na2CO3溶液 | 浓硫酸 |
| B | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 固体NaOH |
| C | Cl2 | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 浓硫酸 |
| D | NO2 | 浓HNO3 | 铜屑 | H2O | 固体NaOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器 | 甲 | 乙 | 丙 |
| 相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
| 反应物投料 | 1mol A2、3mol B2 | 2mol AB3 | 2mol AB3 |
| 平衡时容器体积 | V甲 | V乙 | V丙 |
| 反应的平衡常数K | K甲 | K乙 | K丙 |
| 平衡时AB3的浓度/mol•L-1 | c甲 | c乙 | c丙 |
| 平衡时AB3的反应速率/mol•L-1•min-1 | v甲 | v乙 | v |
| A. | v甲=v丙 | B. | c乙>c甲 | C. | V甲>V丙 | D. | K乙<K丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
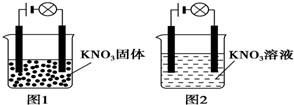
| A. | KNO3不是电解质 | |
| B. | KNO3溶液是电解质 | |
| C. | KNO3在水溶液中电离出了可以自由移动的离子 | |
| D. | 在KNO3溶液中,水电离出了大量的离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com