
除去某溶液里溶解的少量杂质,下列做法中不正确的是(括号内的物质为杂质)
A. NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热
B. KNO3溶液(AgNO3):加过量KCl溶液,过滤
C. Na2SO4溶液(Br2):加CCl4,萃取,分液
D. NaHCO3溶液(Na2CO3):通入足量的CO2
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源:2016-2017学年河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:实验题
已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。
某化学小组根据上述反应原理进行下列实验:
Ⅰ.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol·L-1KMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会________(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为________。
(4)计算H2C2O4溶液的物质的量浓度为________mol·L-1。
Ⅱ.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1mol·L-1KMnO4溶液 | 0.1mol·L-1H2C2 O4溶液 | 0.1mol·L-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中V1=________,V2=________。
(6)实验中需要测量的数据是________。
(7)实验中________(填“能”或“不能”)用0.2mol·L-1盐酸代替0.1mol·L-1H2SO4溶液,理由是________。
查看答案和解析>>
科目:高中化学 来源:2017届河南省濮阳市高三第一次模拟考试理综化学试卷(解析版) 题型:实验题
某研究性学习小组的同学通过查阅资料得到如下信息:草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,受热脱水、升华,易溶于水,170℃以上分解可得到CO、CO2、H2O,H2C2O4难溶于水。他们欲利用如下装置验证上述产物(加热仪器、夹持仪器省略)。
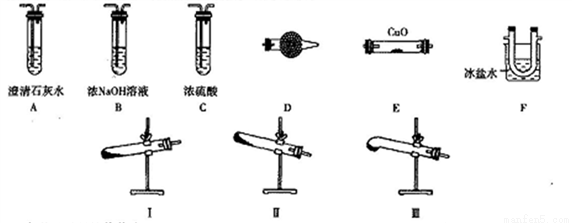
(1)加热草酸晶体使其分解的装置是________(从I、II、III中选取),验证其分解产物的装置依次是______→A→尾气处理装置(用装置字母作答,装置可重复使用)。
(2)D中试剂是_________,证明有CO生成的现象是_______。
(3)实验中有两处需要加热,加热的顺序是_________,写出一种处理尾气的方法:_____________。
(4)若上述实验均产生了预期的现象,写出草酸分解的化学方程式:_________________。
(5)设计一种方案证明草酸是弱酸_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于物质的检验说法不正确的是
A. 向待测液中加入氯化钡溶液,有白色沉淀生成,再加稀硝酸,沉淀不消失,则待测液中一定含有SO42-
B. 观察钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,置于煤气灯的外焰上进行灼烧,透过蓝色钴玻璃进行观察
C. 向待测液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则待测液中一定含有NH4+
D. 向待测液中加入氯化钡溶液,有白色沉淀生成,再加入盐酸,沉淀消失且产生无色无味的气体,则待测液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列各组物质能相互反应得到Al(OH)3的是
A. Al跟NaOH溶液
B. Al(NO3)3跟过量的NaOH溶液
C. Al2O3和水共热
D. Al2(SO4)3和过量的氨水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列实验操作正确的是( )
A. 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中
B. 过滤操作时,为了加快过滤速率,可用玻璃棒不断搅拌过滤器中液体
C. 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液
查看答案和解析>>
科目:高中化学 来源:2017届海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:填空题
镁化合物具有广泛用途。请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的____,还生成少量的______(填化学式);
(2)CH3MgCl是一种重要的有机合成试剂,其中镁的化合价是___________,该化合物水解的化学方程式为____________;
(3)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
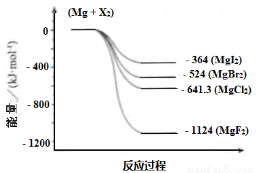
下列选项中正确的是_____________(填序号)。
① MgI2中Mg2+ 与I- 间的作用力小于MgF2中Mg2+ 与F- 间的作用力
② Mg与F2的反应是吸热反应
③ MgBr2与Cl2 反应的△H > 0
④ 化合物的热稳定性顺序为MgI2 < MgBr2 < MgCl2 < MgF2
⑤ MgF2(s) + Br2(l) = MgBr2(s) + F2(g) △H = +600 kJ · mol-1
查看答案和解析>>
科目:高中化学 来源:2017届四川外语学院重庆第二外国语学校高三下学期第二次检测理科综合化学试卷(解析版) 题型:填空题
二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
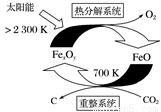
(1)科学家提出由CO2制取C的太阳能工艺如上图所示。
①若“重整系统”发生的反应中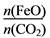 =6,则FexOy的化学式为________。
=6,则FexOy的化学式为________。
②“热分解系统”中每分解1molFexOy,转移电子的物质的量为________。
工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OCH3(g)+H2O(g)===2CH3OH(g) ΔH2=+23.4kJ·mol-1
则2CO2(g)+6H2(g)===CH3OCH3(g)+3H2O(g) ΔH3=________kJ·mol-1。
①一定条件下,上述合成甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是________(填字母)。
a.逆反应速率先增大后减小 b.H2的转化率增大
c.反应物的体积百分含量减小 d.容器中的 值变小
值变小
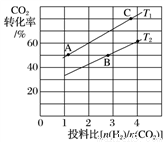
②在某压强下,合成甲醚的反应在不同温度、不同投料比时,CO2的转化率如下图所示。T1温度下,将6molCO2和12molH2充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=__________;KA、KB、KC三者之间的大小关系为____________。
(3)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中,c(NH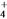 )________(填“>”、“<”或“=”)c(HCO
)________(填“>”、“<”或“=”)c(HCO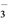 );反应NH
);反应NH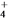 +HCO
+HCO +H2O=NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
+H2O=NH3·H2O+H2CO3的平衡常数K=__________。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省葫芦岛市高三上学期第二次周考理综化学试卷(解析版) 题型:实验题
I.高铁酸钾( K2Fe04)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图1是高铁电池的模拟实验装置:
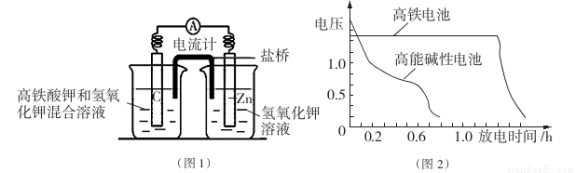
(1)该电池放电时正极的电极反应式为 ;若维持电流强度为1A,电池工作十分钟,理论消耗Zn g(已知F="96500" C/mol)。
(2)盐桥中盛有饱和KC1溶液,此盐桥中氯离子向 移动(填“左”或“右”);若用阳离子交换膜代替盐桥,则钾离子向 移动(填“左”或“右”)。
(3)图2为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
Ⅱ.工业上湿法制备K2Fe04的工艺流程如图3。
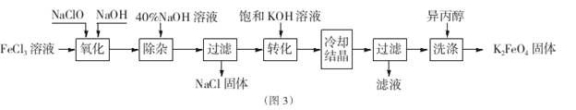
(4)完成“氧化”过程中反应的化学方程式:
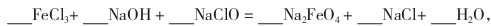
其中氧化剂是 (填化学式)。
(5)加入饱和KOH溶液的目的是
(6)已知25℃时Ksp[Fe(OH)3]=4.0×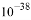 ,此温度下若在实验室中配制5mol/L l00mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入 mL 2 mol/L的盐酸(忽略加入盐酸体积)。
,此温度下若在实验室中配制5mol/L l00mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入 mL 2 mol/L的盐酸(忽略加入盐酸体积)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com