
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3 mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下图为H2CO3在加入强酸或强碱溶液溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:
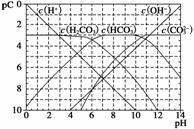
(1)在人体血液中,HCO 能起到使人体血液pH保持在7.35~7.45的作用。
能起到使人体血液pH保持在7.35~7.45的作用。
①请用电解质溶液中的平衡解释:__________________(用离子方程式表示)。
②正常人体血液中,HCO 的水解程度________电离程度(填“<”、“>”或“=”)。
的水解程度________电离程度(填“<”、“>”或“=”)。
③pH=7.00的血液中,c(H2CO3)________c(HCO )(填“<”、“>”或“=”)。
)(填“<”、“>”或“=”)。
(2)H2CO3一级电离平衡常数的数值Ka1≈________。
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO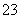 不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确______________________。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1、c(CO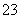 )=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
)=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
答案 (1)①HCO H++CO
H++CO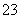 、HCO
、HCO +H2OH2CO3+OH- ②> ③< (2)10-6 (3)用pH试纸(或pH计)测常温下0.1 mol·L-1 Na2CO3溶液的pH,若pH<12,该同学的观点正确;若pH>12,则该同学的观点错误
+H2OH2CO3+OH- ②> ③< (2)10-6 (3)用pH试纸(或pH计)测常温下0.1 mol·L-1 Na2CO3溶液的pH,若pH<12,该同学的观点正确;若pH>12,则该同学的观点错误
(4)c(Li+)=0.075 mol·L-1、c(CO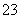 )=0.1 mol·L-1,c2(Li+)·c(CO
)=0.1 mol·L-1,c2(Li+)·c(CO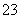 )=5.6×10-4<1.68×10-3,所以无沉淀产生。
)=5.6×10-4<1.68×10-3,所以无沉淀产生。
解析 (1)①依据信息抓住HCO 既能水解也能电离分析;②由信息可知正常人体血液显碱性,所以HCO
既能水解也能电离分析;②由信息可知正常人体血液显碱性,所以HCO 的水解大于电离;③由图像可知c(H2CO3)=c(HCO
的水解大于电离;③由图像可知c(H2CO3)=c(HCO )时溶液显酸性,显中性时c(HCO
)时溶液显酸性,显中性时c(HCO )>c(H2CO3)。(2)Ka1=
)>c(H2CO3)。(2)Ka1= ,pH=6时,c(H2CO3)=c(HCO
,pH=6时,c(H2CO3)=c(HCO ),所以Ka1=c(H+)。(3)由CO
),所以Ka1=c(H+)。(3)由CO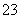 +H2OHCO
+H2OHCO +OH-可知测一定浓度的Na2CO3溶液中c(OH-)即可求出已水解的Na2CO3的浓度。(4)注意最后溶液的体积为原体积的2倍。
+OH-可知测一定浓度的Na2CO3溶液中c(OH-)即可求出已水解的Na2CO3的浓度。(4)注意最后溶液的体积为原体积的2倍。


科目:高中化学 来源: 题型:
氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中[H+]的增大而加快。
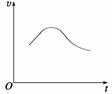
(1) 反应开始时反应速率加快的原因是
________________________________________________________________________
________________________________________________________________________
________________;
(2) 反应后期反应速率减慢的原因是
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列几种物质:①NH3·H2O ②NH4Cl
③(NH4)2SO4 ④NH4HSO4 ⑤NH4HCO3
⑥Na2CO3 ⑦NaHCO3 ⑧NaOH
按要求回答问题:
(1)能促进水的电离且溶液呈酸性的是________。
(2)同浓度的①~④的溶液中c(NH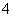 )由大到小的顺序是____________________。
)由大到小的顺序是____________________。
(3)常温下,同浓度⑤~⑧溶液,pH由小到大的顺序是________________。
(4)NaHCO3溶液显碱性的原因是___________________________________________________。
(5)NaHCO3溶液的电荷守恒式:____________________________________________________;
NaHCO3溶液的物料守恒式:______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯碱工业中电解饱和食盐水时,用盐酸控制阳极区溶液的pH在2~3,用化学平衡移动原理解释盐酸的作用_____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知温度T时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=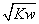 mol·L-1
mol·L-1
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知相同温度下电离常数K(HF)>K(HCN),在物质的量浓度均为0.1 mol·L-1的NaCN和NaF混合溶液中,下列排序正确的是( )
A.c(OH-)>c(HF)>c(HCN)>c(H+)
B.c(OH-)>c(CN-)>c(F-)>c(H+)
C.c(OH-)>c(F-)>c(CN-)>c(H+)
D.c(F-)>c(OH-)>c(HCN)>c(HF)
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1 的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是( )
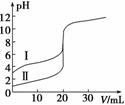
A.Ⅱ表示的是滴定醋酸的曲线
B.pH=7时,滴定醋酸消耗的V(NaOH)小于20 mL
C.V(NaOH) =20.00 mL时,两份溶液中c(Cl-)=c(CH3COO-)
D.V(NaOH) =10.00 mL时,醋酸溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
国际能源网报道:金属燃料可能成为新能源,可能带来结束化石能源时代的希望,是一种理想的储能方式。下列说法不正确的是( )
A.纳米金属燃料,更易点燃
B.铁作燃料时,可用磁性材料吸引生成物,便于产物分离
C.镁可以通过2Mg+CO2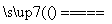 2MgO+C,达到既节能减碳又释放能量的效果
2MgO+C,达到既节能减碳又释放能量的效果
D.可从海水中提取氯化镁,并使氯化镁分解获得镁并释放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
化学概念在逻辑上存在如下关系:

对下列概念的说法正确的是( )
A.化合物与电解质属于重叠关系
B.化合物与碱性氧化物属于交叉关系
C.溶液与胶体属于并列关系
D.离子化合物和电解质属于交叉关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com