


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:不详 题型:单选题
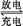 3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,以下说法错误的是( )| A.电池放电是化学能转化成电能的过程 |
B.放电时正极反应为:Fe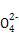 +4H2O+3e- +4H2O+3e-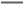 Fe(OH)3+5OH- Fe(OH)3+5OH- |
| C.充电时电池的负极接外电源的正极 |
| D.充电时电解质溶液中的阴离子向阳极定向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
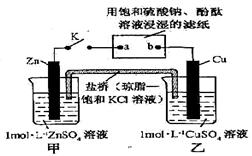
A.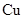 电极上发生还原反应 电极上发生还原反应 |
B.电子沿Zn a a b b Cu路径流动 Cu路径流动 |
| C.片刻后甲池中c(SO42—)增大 |
| D.片刻后可观察到滤纸b点变红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电路中的电子经正极、熔融的K2CO3、负极后再到正极,形成闭合回路 |
| B.电池放电时,电池中CO32-的物质的量将逐渐减少 |
| C.正极反应为2H2O+O2+4e-===4OH- |
| D.放电时CO32-向负极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
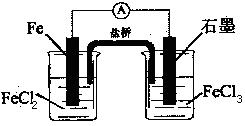
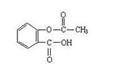
A.该电池负极反应为:2Fe2+-2e-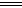 2Fe3+ 2Fe3+ |
| B.当有6.02×1023电子转移时,Fe电极减少56g |
| C.石墨电极上发生氧化反应 |
| D.盐桥中K+移向FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱性电解质溶液中正极反应式为:4OH-- 4e-= O2↑+2H2O |
| B.碱性或酸性电解质溶液中,该电池正极反应式相同 |
| C.该电池工作时,Na+移向负极 |
| D.每生成1 mol ZnO22-转移电子数为2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
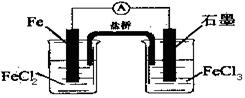
A.该电池负极反应为:2Fe2+-2e- 2Fe3+ 2Fe3+ |
| B.当有6.02×1023电子转移时,Fe电极减少56g |
| C.石墨电极上发生氧化反应 |
| D.盐桥中K+移向FeCl3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com