
【题目】某铜钴矿石主要含有CoO(OH)、CoCO3、Cu2(OH)2CO3和SiO2,及一定量的Fe2O3、MgO和CaO等。由该矿石制Co2O3的部分工艺流程如下:
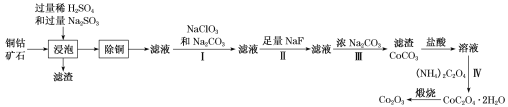
回答下列问题:
(1)“浸泡”过程中,钴(III)可转化为CoSO4,写出该转化的化学方程式:________。
(2)“除铜”若选用MnS,计算常温下该“除铜”反应的平衡常数K=________。[保留2位有效数字;已知常温下Ksp(MnS)=2.5×10–13,Ksp(CuS)=1.3×10–36]
(3)①步骤I中加入NaClO3反应的离子方程式为_______。
②常温下,溶液中金属离子(Mn+)的pM[pM=–lgc(Mn+)]随溶液pH变化关系如图所示,设加入NaClO3后,溶液中的c(CO2+)为0.1molL–1,依据如图分析,步骤I中加入Na2CO3调整溶液pH范围为_____。[当c(Mn+)≤10–6 molL–1,即认为该金属离子沉淀完全]

(4)步骤II中加入足量NaF的目的是________。
(5)过滤出的CoC2O42H2O固体经洗涤后,证明固体已洗净的操作为________。
(6)若某工厂用m1kg该铜钴矿石制备了m2kgCo2O3,假设产率为a,则该矿石中钴元素的百分含量为________。
【答案】2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O 1.9×1023 C1O3–+6Fe2++6H+=C1–+6Fe3++3H2O 3~7.6(或3≤pH<7.6) 形成MgF2、CaF2沉淀,除去溶液中的Mg2+、Ca2+ 取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净 ![]()
【解析】
分析流程图,将粉碎的矿石用过量的稀H2SO4和Na2SO3溶液浸泡,目的是将CoO(OH)、CoCO3、Cu2(OH)2CO3等溶解,以提取目标元素,并把+3价Co还原为+2价,此时Fe2O3、MgO和CaO等也会溶解,铁由+3价还原为+2价。除铜步骤除去浸出液中含铜的化合物,之后向溶液中加入NaClO2溶液,将+2价铁氧化为+3价,再加入一定浓度的Na2CO3溶液,过滤,分离出去杂质元素铁,再向滤液中加入足量NaF溶液,将Ca2+、Mg2+转化为CaF2、MgF2除去。向其中的滤液中加入浓Na2CO3溶液得到CoCO3沉淀,再将该沉淀溶解在盐酸中,再加入(NH4)2C2O4溶液,产生CoC2O4·2H2O沉淀,分离出沉淀,将其进行煅烧可得到Co2O3。据此分析解答。
(1)浸泡过程中为CoO(OH)与稀H2SO4、Na2SO3反应生成CoSO4的过程,根据原子守恒和电子得失守恒可得反应方程式为:2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O;答案为:2CoO(OH)+2H2SO4+Na2SO3=2CoSO4+Na2SO4+3H2O;
(2)用MnS“除铜”,发生反应为:MnS(s)+Cu2+(aq)![]() CuS(s)+Mn2+(aq),该反应的平衡常数K=
CuS(s)+Mn2+(aq),该反应的平衡常数K=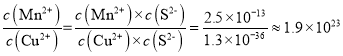 。答案为:1.9×1023;
。答案为:1.9×1023;
(3)①步骤I中加入NaClO3,是Fe2+与NaClO3反应,被氧化生成Fe3+,反应的离子方程式为:C1O3–+6Fe2++6H+=C1–+6Fe3++3H2O;答案为:C1O3–+6Fe2++6H+=C1–+6Fe3++3H2O;
②步骤Ⅰ中加入Na2CO3调整溶液pH值是为了除去铁元素,根据题给信息,当c(Mn+)≤10–6 molL–1,即认为该金属离子沉淀完全,故需调节pH≥3,即可保证Fe3+沉淀完全,同时不影响Co2+元素,需pH<7.6,则Na2CO3调整溶液pH范围为:3~7.6(或3≤pH<7.6);答案为:3~7.6(或3≤pH<7.6);
(4)步骤II中加入足量NaF,可将滤液中存在的Ca2+、Mg2+转化为CaF2、MgF2沉淀而除去,故步骤II中加入足量NaF的目的是:形成MgF2、CaF2沉淀,除去溶液中的Mg2+ 、Ca2+;答案为:形成MgF2、CaF2沉淀,除去溶液中的Mg2+ 、Ca2+;
(5)CoC2O42H2O晶体表面附着Cl-和NH4+,为看到明显现象应检验Cl-,可通过检验沉淀洗涤液中是否存在Cl-来判断沉淀是否洗涤干净,具体操作为:取少量最后一次洗涤液于试管中,加入硝酸酸化的硝酸银溶液,若无白色沉淀产生,则证明已洗净;
(6)设钴在该铜钴矿石中的百分含量为x,则![]() ,即
,即![]() 。答案为:
。答案为:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】有机物甲是乙(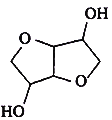 )的同分异构体(不考虑立体异构),1.460g甲与足量饱和碳酸氢钠溶液反应,放出448 mL CO2(标准状况下),下列说法错误的是
)的同分异构体(不考虑立体异构),1.460g甲与足量饱和碳酸氢钠溶液反应,放出448 mL CO2(标准状况下),下列说法错误的是
A.甲的分子式为C6H10O4
B.甲与乙可以发生酯化反应
C.乙的一氯代物有3种
D.甲可能的结构共有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 A 是单质,A、B、C、D、E 五种物质均含同一种元素,X 是地壳中含量最多的元素形成的单质,相互转化关系如图所示.回答下列问题:

(1)通常情况下,若A为气体,C、D都是大气污染物;
①写出下列反应的化学方程式
B![]() C_________________
C_________________
E![]() C_________________
C_________________
②实验室中检验B的操作方法是_________________。
③标准状况下,将盛满D的试管倒扣在盛满水的水槽中,一段时间后,假定溶质不扩散,则试管中所得溶液的物质的量浓度为____________。
(2)通常情况下,若A为淡黄色固体:
①写出B与C反应的化学方程式:_______________________。
②将C通入溴水中的现象是______,发生反应的离子方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是p能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E的单质是常温下唯一呈液态的非金属。请回答下列问题:
(1)X、Y、Z第一电离能由小到大的顺序为__________(填元素符号)。Y的氢化物的分子空间构型是_______。其中心原子采取_____杂化,属__________(填“极性”或“非极性”)分子。
(2)E元素基态原子的电子排布式为_______________________________。
(3)XZ2分子中含有________个π键。
(4)Z氢化物的沸点比Q氢化物的沸点高,理由是____________________________。
(5)X元素可形成X60单质,它与金属钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),该化合物中X60与钾原子个数比为___________。
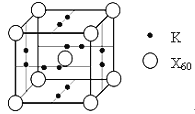
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组拟利用如图装置制取干燥的氮气。下列说法错误的是( )

A.装置I中发生的反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B.加热片刻后需要将酒精灯移开,说明该反应是放热反应
C.装置II的作用是冷凝水蒸气
D.在装置III末端收集纯净干燥的N2只能用向下排空气法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pC类似于pH,是指极稀溶液中溶质浓度的负对数。常温下向H2CO3溶液中逐滴滴加NaOH溶液,测得溶液的pC与pH关系如图所示。下列说法错误的是( )
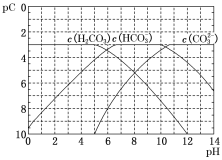
A.在同一溶液中,H2CO3、HCO3–、CO32–不能大量共存
B.H2CO3二级电离平衡常数Ka2的数量级等于10–11
C.当pH=7时,溶液中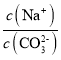 >3
>3
D.向H2CO3溶液滴加NaOH溶液至溶液呈中性的过程中,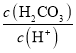 逐渐变小
逐渐变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
2 C(g)+2D(g) ΔH=Q, 2 min末达到平衡,生成0.8 mol D。
(1)300℃时,该反应的平衡常数表达式为K=______________,已知K300℃<K350℃,则ΔH____0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应由两步反应A→B、B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能)。下列有关叙述正确的是

A. 两步反应均为吸热反应 B. 三种化合物中C最稳定
C. 加入催化剂会改变反应的焓变 D. 整个反应的ΔH=E1-E2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com