
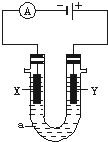
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:分析 (1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)根据电镀的工作原理知识来回答,电解方法镀银,电解池的阴极材料是镀件铁,阳极为金属银;
(3)若用电解方法防止铁被腐蚀应做电解池的阴极.
解答 解:(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,
故答案为:2H++2e-=H2↑;电极上放出气体,溶液变红;
②和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,氯气能使湿润的碘化钾淀粉试纸变蓝,可以用于氯气的检验,电解饱和食盐水发生反应生成氢气、氯气和氢氧化钠,反应的化学方程式为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2Cl--2e-=Cl2↑;把湿润的碘化钾淀粉试纸放在Y电极附近,试纸变蓝色,说明有氯气生成;2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(2)电解方法镀银,电解池的阴极材料是镀件铁,阳极为金属银,电解质溶液为:AgNO3(或可溶性银盐),
故答案为:AgNO3(或可溶性银盐),铁件;
(3)若用电解方法防止铁被腐蚀应做电解池的阴极被保护,所以铁做X电极,
故答案为:X.
点评 本题考查学生电解池的工作原理知识,可以根据所学知识进行回答,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的干馏是物理变化 | |
| B. | 煤的气化和液化主要目的是为了获得较洁净的能源 | |
| C. | 汽油主要来自石油的裂解 | |
| D. | 乙烯是来自石油的裂化和裂解的重要化工原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
| 加硫酸的次数序号 | 加入硫酸的体积/mL | 剩余固体的质量/g |
| 1 | 20.0 | 7.20 |
| 2 | 20.0 | 4.40 |
| 3 | 20.0 | 2.00 |
| 4 | 20.0 | 2.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 124g P4含有的P-P键的个数为3NA | |
| B. | 18g冰晶体中含有的氢键的个数为4NA | |
| C. | 12g金刚石中含有的C-C键的个数为4NA | |
| D. | 60gSiO2中含Si-O键的个数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某温度时,在容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中的数据分析:该反应的化学方程式为3X+Y?2Z.
某温度时,在容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中的数据分析:该反应的化学方程式为3X+Y?2Z.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com