
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B、核外电子排布相同的微粒化学性质相同 |
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D、还原性强弱:F-<Cl-<I- |


科目:高中化学 来源: 题型:
| A、依据丁达尔现象可区分氯化钠溶液和蛋白质溶液 |
| B、仅由同一种元素组成的物质一定是纯净物 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、Na2O2能与CO2反应产生O2,可用作高空飞行或潜水的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、CuFeS2只作还原剂 |
| B、Fe元素全部被氧化 |
| C、还原产物是Cu、FeO、Fe2O3和SO2 |
| D、若生成1molCu,则反应中转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 |
| B、SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同 |
| C、用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 |
| D、用AgNO3溶液可以鉴别KCl和KI |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )| 选项 | a中的物质 | b中的物质 | C中收集的气体 | d中的物质 |
| A | 浓氨水 | CaO | NH3 | H2O |
| B | 稀硝酸 | Cu | NO2 | H2O |
| C | 稀硝酸 | FeS | H2S | NaOH溶液 |
| D | 浓盐酸 | KMnO4 | Cl2 | NaOH溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol?L-1 |
| B、若V1=V2,反应后溶液的pH一定等于7 |
| C、若反应后溶液呈酸性,则V1一定大于V2 |
| D、若反应后溶液呈碱性,则V1一定小于V2. |
查看答案和解析>>
科目:高中化学 来源: 题型:
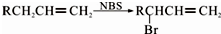 .
.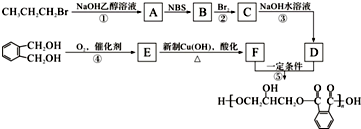
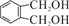 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨水 | B、NaOH溶液 |
| C、稀硫酸 | D、浓硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com