
| A、溶液中可能发生:Z2+2A2+═2A3++2Z- |
| B、Z2在①、③反应中均为氧化剂 |
| C、氧化性强弱顺序为:XO4->Z2>B2>A3+ |
| D、X2+是XO4-的还原产物 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑥⑦ | B、①④⑤ |
| C、③⑦⑧ | D、③⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、1:2 |
| C、2:3 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾溶于水后,铝离子发生水解,生成氢氧化铝胶体 |
| B、氢氧化铝胶体因吸附溶液中的阳离子而带正电荷 |
| C、带正电荷的氢氧化铝胶粒能吸附水中杂质,并使这些杂质与氢氧化铝胶体一起凝聚而沉降 |
| D、天然水经明矾处理后可除去水中的杂质和细菌,就可以饮用了 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷的分子式:CH3CH3 |
B、CH4分子的球棍模型: |
| C、乙烯的结构简式:CH2=CH2 |
D、苯乙醛结构简式: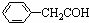 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com