
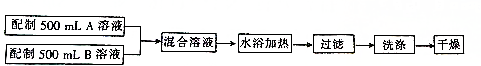
分析 (1)过滤时玻璃棒的作用是引流,向置于过滤器上的沉淀加蒸馏水至完全浸没沉淀,静置,重复此操作三次;
(2)依据n=cV计算NaOH的质量,c=$\frac{n}{V}$计算B溶液中c(Na+);
(3)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+$\frac{3}{2}$b+$\frac{1}{2}$c)H2O+dCO2↑,计算耗酸量.
解答 解:(1)过滤时玻璃棒的作用是引流,洗涤步骤的操作方法是:把沉淀置于过滤器中,加入蒸馏水浸没沉淀,待水自然流下,重复此操作三次,
故答案为:引流;把沉淀置于过滤器中,加入蒸馏水浸没沉淀,待水自然流下,重复此操作三次;
(2)因为B溶液为c(NaOH)=1.6mol•L-1和c(Na2CO3)=0.8mol•L-1的混合溶液,则NaOH的质量m=40n=40cV=40×1.6×0.5=32.0g,c(Na+)=$\frac{n}{V}$=$\frac{1.6×0.5×+0.8×0.5×2}{0.5}$=3.2mol•L-1,
故答案为:32.0g;3.2;
(3)据方程式:MgaAlb(OH)c(CO3)d+(2a+3b)HCl=bAlCl3+aMgCl2+(a+$\frac{3}{2}$b+$\frac{1}{2}$c)H2O+dCO2↑,
1 (2a+3b) d
1mol水滑石消耗(2a+3b)mol盐酸,则0.1mol水滑石消耗(0.2a+0.3b)mol盐酸,消耗盐酸体积为:$\frac{(0.2a+0.3b)mol}{1mol/L}$=(0.2a+0.3b)L,
故答案为:0.2a+0.3b.
点评 本题考查了配制一定物质的量浓度的溶液的方法及其计算,明确配制原理和过程是解题关键,注意基本公式的应用,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 锗是一种金属性很强的元素 | B. | 锗的单质具有半导体的性能 | ||
| C. | 锗化氢(GeH4)稳定性很强 | D. | 锗酸(H4GeO4)是难溶于水的弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | O2+4H++4e-=2H2O | B. | O2+2H2O+4e-=4OH- | ||
| C. | N2H4+4OH--4e-=N2+4H2O | D. | N2H4+4H++2e-=2NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时向水中加入少量固体CH3COONa,平衡逆向移动,c (H+)降低,Kw不变 | |
| B. | 由水电离出的c(H+)=10-12mol•L-1的溶液中:Na+、Ba2+、HCO3-、Cl-可以大量共存 | |
| C. | 向Na2CO3溶液中加入NaOH溶液后,c(CO32- )减少 | |
| D. | 某温度时的混合溶液中c(H+)=$\sqrt{{K}_{W}}$mol•L-1,说明该溶液呈中性(KW为该温度时水的离子积常数) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=14的溶液 | |
| B. | c(OH-)=1.0×10-13mol•L-1的溶液 | |
| C. | 0.6%的醋酸(ρ=1g•cm-3) | |
| D. | pH=2的盐酸与pH=12的氢氧化钡溶液等体积混合后所得溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 带相反电荷离子之间的静电作用称为离子键 | |
| B. | 金属元素与非金属元素化合时,不一定形成离子键 | |
| C. | 某元素的原子最外层只有一个电子,它跟卤素结合时所形成的化学键不一定是离子键 | |
| D. | 非金属元素形成的化合物中不可能含有离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com