
| A. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| B. | 用乙醚从黄花蒿中提取青蒿素是利用了氧化还原反应原理 | |
| C. | “丹砂(HgS)烧之成水银,积变又成丹砂.”这个过程是可逆反应 | |
| D. | 丁达尔效应可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔效应 |
分析 A.高温下蛋白质发生变性;
B.乙醚从黄花蒿中提取青蒿素,为萃取原理;
C.丹砂(HgS)烧之成水银,积变又成丹砂,化学反应的条件不同;
D.稀硫酸为溶液,云、雾为胶体分散系.
解答 解:A.加热能杀死流感病毒,与蛋白质受热变性有关,故A正确;
B.乙醚从黄花蒿中提取青蒿素,为萃取原理,为物理变化,故B错误;
C.丹砂(HgS)烧之成水银,积变又成丹砂,化学反应的条件不同,二者不是可逆反应,故C错误;
D.稀硫酸为溶液,云、雾为胶体分散系,则云、雾均能产生丁达尔效应,稀硫酸不能,故D错误;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:解答题
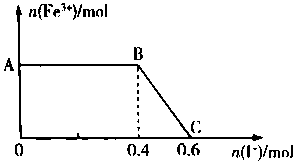 将FeC12溶液与过量氯水(视溶质为Cl2)混合,发生反应:Cl2+ZFeCl2=2FeCl3,得到溶液X.向溶液X中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.已知Cl2、FeCl3均可将I-氧化为I2,其自身分别被还原为Cl-、Fe2+.回答下列问题:
将FeC12溶液与过量氯水(视溶质为Cl2)混合,发生反应:Cl2+ZFeCl2=2FeCl3,得到溶液X.向溶液X中加入KI溶液,混合溶液中Fe3+的物质的量随加入KI的物质的量的变化关系如图所示.已知Cl2、FeCl3均可将I-氧化为I2,其自身分别被还原为Cl-、Fe2+.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LNa2SO3溶液中:c(Na+)═2c(SO32-)+c(HSO3-)+c(H2SO4)=0.2mol/L | |
| B. | 常温下pH=a的稀H2SO4与pH=b的氨水等体积混合后恰好完全反应,则a+b<14 | |
| C. | 0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:c(H+)-c(OH-)═c(CH3COO-)-c(CH3COOH) | |
| D. | pH相同的三种溶液①NH4Cl ②(NH4)2SO4 ③NH4HSO4,c(NH4+)大小关系为:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA | |
| B. | 12gNaHSO4固体中含阳离子数为0.1NA | |
| C. | 标准状况下,22.4LBr2中所含分子数为NA | |
| D. | 7.8gNa2O2与足量的水反应转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4既能使溴水褪色,也能使酸性KMnO4溶液褪色 | |
| B. | 蔗糖和葡萄糖属于同系物 | |
| C. | 用碳酸钠溶液可以区别出乙酸、乙醇和苯三种液体 | |
| D. | 苯乙烯的所有原子都可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②③ | B. | ④②①③ | C. | ③②①④ | D. | ④②③②① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com