
| A. | 胶体的电泳 | B. | 血液的氧化还原反应 | ||
| C. | 血液中发生复分解反应 | D. | 胶体的聚沉 |
分析 胶体在遇到电解质溶液、加热、电性相反的电解质的时候都会聚沉,结合题目中所给信息解答即可.
解答 解:A、血液属于胶体,因为没有外接电源,所以不属于电泳现象,故A错误.
B、血液和氯化钠不发生氧化还原反应,故B错误;
C、血液和氯化钠不具备复分解反应的条件,所以不发生复分解反应,故C错误;
D、血液属于胶体,所以血液应具备胶体的性质,在遇到电解质溶液、加热、电性相反的电解质的时候都会聚沉;在伤口上撒盐可以使伤口表面的血液凝结,从而阻止进一步出血,以及防治细菌感染,属于胶体的聚沉,故D正确;
故选D.
点评 本题主要考查的是胶体的性质,了解胶体的性质并与生活中的常见胶体性质的利用是解决本题的关键,难度不大.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L的水所含有的分子数是NA | |
| B. | 常温常压下,11.2L CO2的中所含O原子数为NA | |
| C. | 32g氧气在标准状况下所占的体积与相同条件下NA个N2分子所占的体积相同 | |
| D. | 标准状况下,11.2L NO、NO2混合气体含有的氮原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15N与14N互为同位素 | B. | 13C与C60互为同素异形体 | ||
| C. | 13C、15N具有相同的中子数 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L 乙烯和丙烯的混合气体中分子数为NA | |
| B. | 一定温度下,15 g甲醛和葡萄糖的混合物含O原子数为0.5 NA | |
| C. | 常温常压下,8.8 g乙酸乙酯中含有C-O键的个数为0.5 NA | |
| D. | 4 mL 15 mol•L-1浓硝酸与足量铜反应,生成NO2的分子数约为0.03 NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na218O中氧离子的结构示意图: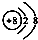 | |
| B. | 比例模型 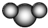 ,表示二氧化碳或水分子 ,表示二氧化碳或水分子 | |
| C. | 碳正离子 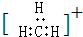 中质子数与电子数之比值为3:2 中质子数与电子数之比值为3:2 | |
| D. | TNT 结构简式: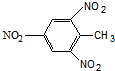 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤>④>③>②>① | B. | ②>①>③>④>⑤ | C. | ②>③>④>①>⑤ | D. | ①>②>③>④>⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 H4SiO4 | B. | Cl2O HClO4 | C. | Mn2O7 HMnO4 | D. | N2O5 HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com